7 Minutės
Reumatoidinis artritas (RA) gali prasidėti gerokai anksčiau nei atsiranda skausmingas sąnarių patinimas. Nauji tyrimai rodo, kad būdingi imuniniai pokyčiai — aptinkami kraujyje metais prieš klinikinį sinovitą — žymi tylųjį etapą, kuriame autoimuninė veikla palaipsniui intensyvėja. Ankstyvų biomarkerių identifikavimas gali pagerinti ligos prognozavimą, suteikti galimybę pradėti gydymą anksčiau ir taip sumažinti progresinį sąnarių pažeidimą, kuris apibrėžia RA.
Fonas: tylus autoimunitetas ir ACPAs
Reumatoidinis artritas yra autoimuninė liga, kai imuninė sistema klaidingai atakuoja sąnarių audinius, sukeldama lėtinį uždegimą, skausmą ir progresuojantį audinių pažeidimą. Klinikinėmis apraiškomis matomas sąnarių uždegimas vadinamas sinovitu. Tačiau prieš atsirandant akivaizdiems sinovito požymiams, kai kurie asmenys jau būna aptikę specifinių autoantikūnų kraujyje — anticitrulinuotų baltymų antikūnų (ACPAs) — kurie yra stiprus RA rizikos žymuo.
ACPAs nėra vienintelė biologinė priežastis, tačiau jų buvimas ženklina autoimuninės reakcijos pradžią organizme. Svarbu pažymėti, kad ACPA teigiamumas padidina RA riziką, bet dauguma ACPA teigiamų žmonių iš karto neperauga į aktyvią ligą. Todėl išliko neaišku, kokie biologiniai žingsniai ir kokiu metu veda nuo „tylaus“ autoimuniteto prie klinikinio reumatoidinio artrito.
Šioje ankstyvoje fazėje veikia sudėtingas molekulinių ir ląstelinių mechanizmų tinklas: nuo baltymų citrulinacijos audiniuose, antigenų pateikimo, B ląstelių diferencijacijos į antikūnus gaminančias plasmocitas, iki T limfocitų vaidmens B ląsteles užtikrinančiuose procesuose. Genetiniai veiksniai (pvz., „shared epitope“) ir aplinkos rizikos veiksniai (pvz., rūkymas arba tam tikros burnos ir kvėpavimo takų infekcijos) taip pat prisideda prie ankstyvųjų imuninių pokyčių ir ACPA atsiradimo.
Tyrimo dizainas ir metodai
JAV tyrėjų grupė, vadovaujama Allen Institute for Immunology, California University San Diego ir University of Colorado Anschutz, sekė ACPA teigiamus asmenis, siekdama žingsnis po žingsnio užfiksuoti imuninės sitemos pokyčius, kurie išankstinai sudaro sąlygas RA išsivystymui. Kohorta apėmė 45 asmenis, priskirtus rizikos grupei dėl ACPA aptikimo kraujyje; iš jų 16 vėliau diagnozuotas klinikinis RA. Tyrime taip pat naudoti sveikų kontrolinių asmenų duomenys, kad būtų galima palyginti ir išskirti specifinius signalus.
Tyrėjai naudojo kelių tipų aukštaplečiausias analizės technologijas: kraujo proteomiką (kad būtų kiekybiškai įvertinti uždegiminiai baltymai), detalų imuninės ląstelių profiliavimą (įskaitant vienaląstelinio lygmens fenotipavimą) ir funkcines B bei T limfocitų analizes. Tokiu būdu sukurtas laiko juostos modelis, fiksuojantis, kaip keičiasi proteominis ir ląstelinės imuninės reakcijos kraujyje per priešinį etapą iki klinikinės ligos pradžios.
Metodologiškai tai apėmė ilgesnį laikotarpį trunkančius longitudinalius mėginių ėmimus, duomenų integraciją ir statistinį modeliavimą, leidžiantį atskirti nuolatinius nuo pereinamų signalų. Naudotos priemonės apėmė masinės spektrometrijos pagrindu grįstą proteomiką, daugiamatį imuninį fenotipavimą (pvz., tokias technologijas kaip masinė citometrija ar vienaląstelinė transkriptomika), bei funkcinės klasifikacijos testus, vertinančius citokinų gamybą ir antikūnų aktyvumą.
Pagrindinės išvados
Tyrimas atskleidė aiškų uždegiminių baltymų ir imuninės veiklos padidėjimą ACPA teigiamuose dalyviuose, palyginti su kontrolėmis. Ypač padidėjo baltymai, susiję su tiek įgimtu, tiek adaptaciniu imunitetu — tokie signalai rodo intensyvesnį antigenų atpažinimą, citokinų tinklo aktyvaciją ir ląstelinį budrumą tolimesnei autoimuninei grandinei vykdyti.
Detalesnė limfocitų analizė parodė, kad tiek B ląstelės (antikūnus gaminančios ląstelės), tiek T ląstelės (kurios koordinuoja B ląstelių atsaką) linko į labiau „paruoštą“ arba „primed“ būseną. Tai reiškia, kad ląstelės rodė fenotipinius ir funkcinius pakitimus, kurie sumažina jų slenkstį reaguoti į antigenus. Artėjant prie RA diagnozės datos, dažnis tų T ir B ląstelių padidėjo — ypač tų populiacijų, kurios poliarizuojasi į uždegimines funkcijas, net jeigu kai kurios iš jų tradiciškai laikomos mažiau uždegiminėmis.
Pavyzdžiui, pastebimas padidėjimas plasmablastų ir tam tikrų T pagalbinio tipo ląstelių (pvz., folikulinio T pagalbinio fenotipo) dalyje asmenų, kurie vėliau išsivystė į RA. Taip pat aptikti interferono signalizacijos ir TNF/IL-6 susijusių kelių sustiprėjimo požymiai kraujyje, kas sutampa su ankstyvuoju sisteminiu uždegimu prieš aiškų sąnarių uždegimą.
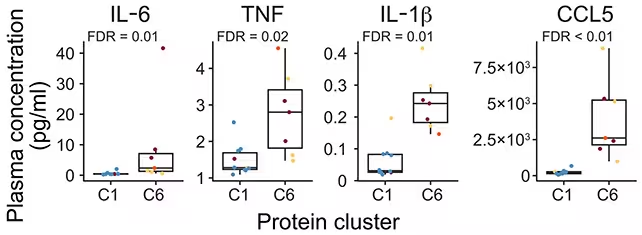
Uždegiminiai baltymai buvo labiau paplitę grupėje, sudarytoje daugiausia iš artrito rizikos turinčių asmenų (C6). (He et al., Sci. Transl. Med., 2025)
Nors tarp tų, kurie progresavo į RA, ir tų, kurie neprogresavo, egzistavo persidengimo zona, išryškėjo uždegimo „parašas“, apibūdinantis, kaip biologiniai pokyčiai priešinėje stadijoje evoliucionuoja į klinikinę ligą. Autoriai pažymi: „Mūsų rezultatai palaiko koncepciją, kad RA uždegiminė liga prasideda gerokai anksčiau nei aktyvaus sinovito atsiradimas, ankščiau negu tai yra kliniciškai pastebima.“
Reikšmė diagnostikai ir gydymui
Gilesnis supratimas, kurie imuniniai signalai iš anksto praneša apie progresą į RA, atveria kelias naudingas galimybes. Pirma, uždegiminių baltymų ir imuninės ląstelių žymenų rinkiniai gali praturtinti rizikos stratifikaciją tarp ACPA teigiamų asmenų, suteikdami tikslesnę prognozę nei vien tik antikūnų statusas. Tokie biomarkeriai galėtų padėti atskirti asmenis, kuriems gresia greitesnis perėjimas į simptominę ligą, nuo tų, kurių rizika yra žemesnė ir kur pakanka išsamaus stebėjimo.
Antra, intervencijos, nukreiptos į šį preklininį langą, galėtų užkirsti kelią sinovitui arba jį atitolinti, taip sumažinant ilgalaikį sąnarių pažeidimą. Vienas iš pavyzdžių — abataceptas (CTLA‑4 Ig), imunomoduliatorius, kuris jau naudojamas tam tikroms aukštos rizikos grupėms ir turi duomenų, rodančių tam tikrų imuninės aktyvacijos aspektų atstatymą. Tai patvirtina idėją, kad tikslinės terapijos gali būti veiksmingos dar prieš pilną ligos išsivystymą.
Tokia prevencinė strategija reikalauja paruoštų klinikinių tyrimų, kuriuose būtų aiškiai apibrėžtos įtraukties kriterijos, saugos profiliai ir ilgalaikiai rezultatai. Be to, svarbu apsvarstyti etiką ir sveikatos priežiūros išteklių paskirstymą — kokio laipsnio rizika ir kokia tikimybė išsivystyti RA pateisina ankstyvą gydymo pradžią. Tai ypač aktualu, kai biomarkeriai turi tam tikrą klaidingų teigiamų arba klaidingų neigiamų rezultatų riziką.
Galiausiai, pagerėjęs imuninės architektūros supratimas gali atskleisti naujas biologines tikslines sritis prevenciniam poveikiui — pavyzdžiui, signalizacijos kelius, kurie palaiko B ląstelių diferenciaciją į patogenines plasmacitas, arba T ląstelių apmokymo mechanizmus, kurie skatintų autoimuninį atsaką. Tokie atradimai leidžia sukurti labiau personalizuotas intervencijas, mažinančias nereikalingą bendros imuninės slopinimo riziką.
Kevin Deane, reumatologas iš CU Anschutz, kurį cituoja tyrimo grupė, pažymi, kad šie radiniai gali „palaikyti papildomus tyrimus … siekiant geriau prognozuoti, kas sirgs RA, identifikuoti potencialinius biologinius taikinius RA prevencijai bei rasti būdus tobulinti gydymo strategijas.“
Išvados
Šis darbas žemėlapiuoja RA preklininę fazę, kurią charakterizuoja uždegiminių baltymų kilimas ir vis aktyvesnės B bei T limfocitų populiacijos. Nors gydymo pakeitimams, grindžiamiems šiais biomarkeriais, reikės papildomų klinikinių bandymų ir ilgalaikio saugumo vertinimo, matomų ankstyvųjų signalų identifikavimas nukreipia sritį link proaktyvių, prevencinių strategijų. Tokios priemonės turi potencialą riboti reumatoidinio artrito sukeltą skausmą ir neįgalumą bei pagerinti pacientų ilgalaikę gyvenimo kokybę.
Praktiniu požiūriu seka keli žingsniai: (1) plačiau validuoti atrinktus biomarkerius nepriklausomose kohortose, (2) sukurti klinikinio pritaikymo algoritmus, kurie sujungtų ACPA statusą su proteominiais ir ląstelinių žymenų profiliais, ir (3) suplanuoti gerai valdomus prevencinius klinikinius tyrimus, kurių tikslas — išbandyti, ar ankstyvos intervencijos, tokios kaip imunomoduliatoriai ar tiksline kryptimi veikiantys agentai, gali išvengti arba atitolinti sinovito pradžią be pernelyg didelės žalos pacientui.
Tokiu būdu mokslas ne tik atskleidžia ankstyvas ligos mechanikas, bet ir suteikia aiškų kelio žemėlapį šiuolaikinei, duomenimis pagrįstai reumatoidinio artrito prevencijai ir valdymui.
Šaltinis: sciencealert

Palikite komentarą