8 Minutės
Įsivaizduokite sužinoję, kad esate kelyje link demencijos dar prieš pirmuosius pastebimus simptomus — užmirštą vardą ar praraktą raktą. Tą pažadą teikia naujas, iš pažiūros paprastas kraujo testu paremtas „molekulinis laikrodis“, kuris gali susiaurinti tikėtiną Alzheimerio simptomų atsiradimo langą iki trijų–keturių metų.
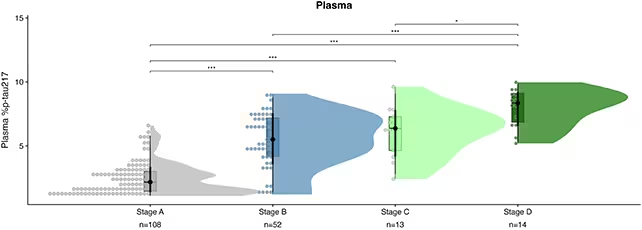
p‑tau217 baltymo lygiai parodyti koreliaciją su Alzheimerio progresavimu.
Kaip baltymas kraujyje žemėlapiuoja smegenų pokyčius per metus
Vašingtono universiteto Sent Luise mokslininkai adaptavo jau egzistuojantį p‑tau217 kraujo tyrimą ir papildė jį matematiniais modeliais. Rezultatas — įrankis, kuris susieja išmatuotus baltymo lygius su tašku, kada atminties ir kitų pažinimo funkcijų sutrikimai taps pastebimi. Skamba paprastai. Panaudojimas gali būti reikšmingas.
Kodėl p‑tau217? Šis tau baltymo fosforilintos formos variantas atspindi du pagrindinius Alzheimerio biologinius požymius: susikaupusius tau mazgus (neurofibrilines tangles) ir amyloid‑beta plokšteles. p‑tau217 koncentracija kraujyje atspindi procesus, vykstančius smegenyse, suteikdama langą į ilgalaikę, lėtai besivystančią patologiją be PET skenavimo ar nugaros smegenų skysčio (likvoro) punkcijos sąnaudų ir diskomforto.
Tyrėjai išanalizavo ilgalaikius kraujo duomenis iš 603 dalyvių, surinktus per keletą metų. Braižydami p‑tau217 trajektorijas ir lygindami jas su amžiumi, kuriuo pirmą kartą pasireiškė pažinimo simptomai, jie išvedė formules, kurios padeda nustatyti individo vietą laiko juostoje tarp ankstyviausio biologinio pokyčio ir klinikinio nuosmukio. Paprastai intervalas tarp pirminių smegenų pokyčių ir pastebimo pažinimo sutrikimo yra ilgas — dažnai 10–30 metų — todėl įrankis, susiaurinantis prognozę iki kelių metų, yra vertingas tiek tyrimų planavimui, tiek ateityje pacientų priežiūrai.
Metodologija apima kelis svarbius komponentus: jautrų ir specifinį p‑tau217 imunotyrimą, nuoseklų mėginių surinkimą iš tų pačių dalyvių skirtingais laiko taškais (longitudinalūs duomenys), statistinį trajektorijų modeliavimą ir laiko‑iki‑sintomo estiamtavimą. Matematiniai modeliai gali apimti hierarchinius mišriųjų efektų modelius, survival (gyvenimo trukmės) analizę ir tikimybinius modelius, kurie leidžia transformuoti baltymo lygį į laikytiną laiko langą iki simptomų atsiradimo.
Vis dėlto yra niuansų. Šiuo metu metodas geriausiai veikia grupiniu lygiu. Jis patikimai atskiria kohortas, kurios greičiausiai išsivystys simptomatikoje per apibrėžtą laikotarpį, tačiau dar nesuteikia itin tikslių prognozių atskiram asmeniui. Tyrėjai pabrėžia, jog reikia daugiau duomenų, įvairovės tarp tirtųjų populiacijų ir algoritmo tobulinimo, kad tai taptų rutinine prognozės priemone klinikoje.
Techniniai aspektai ir hipotezės
p‑tau217 yra tau baltymo variantas, kuriame įvykusi fosforilinacija ties treonino pozicija 217 susijusi su specifiniais neurodegeneraciniais procesais. Tyrimuose p‑tau217 lygiai correliuoja tiek su tau agregatais, aptinkamais audiniuose, tiek su amyloid‑beta apnašomis, o tai suteikia biologinį pagrindą, kodėl kraujo biomarkeris atspindi patologiją smegenyse. Laboratoriniai protokolai, siekiant užtikrinti pakartojamumą, apima kontrolines serijas, kalibracijas ir tarpinstitucinius palyginimus, kad p‑tau217 matavimai būtų lyginami tarp centrų.
Duomenų reikalavimai ir modelių validacija
Norint patikimai perkelti molekulinį laikrodį į klinikinę praktiką, reikalinga kelių rūšių validacija: statistinė (ar modelis prognozuoja geriau nei atsitiktinumas), klinikinė (ar prognozės atitinka paciento patirtį ir rezultatą) ir populiacinė (ar modelis veikia skirtingose demografinėse grupėse). Idealiu atveju tolesniuose tyrimuose būtų įtraukti didesni ir demografiškai įvairūs imčių rinkiniai, įvertinamos papildomos kraujo biomarkerių kombinacijos (pvz., amyloid‑beta 42/40 santykis, neurofilamento lengvas grandinę — NfL) ir įtraukiami multimodaliniai duomenys (kognityviniai testai, genetika, neurovaizdavimo rodikliai).
Modeliai, amžiaus įtaka ir kodėl laikrodis svarbus
Pagrindinis autorius Kellen Petersen amyloido ir tau kaupimąsi palygina su medžių metų žiedais. Jei žiedus skaitai neteisingai — suklysti nustatydamas amžių. Jei skaitai teisingai — gali įvertinti, kada medis pradėjo augti. Palyginimas atspindi du dalykus: pirma, kaupimasis vyksta pastovia trajektorija daugeliu atvejų; antra, amžius, kai šie biomarkeriai peržengia patologinį slenkstį, yra stiprus prognozuojantis faktorius, kada pasireikš simptomai.
Vienas reikšmingas atradimas buvo tas, kad vyresniems asmenims intervalas tarp biologinio pokyčio pradžios ir simptomų atsiradimo linko būti trumpesnis. Jaunesnės smegenys gali ilgiau kompensuoti pažeidimus, slėpdamos klinikinius simptomus, net kai patologija kaupiasi. Tai turi tiesioginių pasekmių klinikinių tyrimų dizainui: įtraukiant jaunesnius, biomarkeriais teigiamus dalyvius gali prireikti ilgesnio stebėjimo, kad būtų užfiksuotas simptomų pradžia, tuo tarpu vyresni dalyviai gali rodyti pokyčius greičiau.
Reikšmė klinikiniams tyrimams
Praktinės naudos yra plačios. Prevencinių terapijų klinikiniams tyrimams reikia dalyvių, kurie greičiausiai išsivystys simptomuose tyrimo lango viduje. Kraujo pagrindu veikiantis laikrodis padeda tikslingiau atrinkti tokias puses, taip sumažinant tyrimų dydį ir laikotarpį. Tai ekonominis privalumas — mažesnės išlaidos, greitesni rezultatų gavimai — ir logistinis privalumas: kraujo mėginiai yra lengviau prieinami ir skalaujami nei PET vaizdavimas ar likvoro tyrimai, kurie yra brangūs ir ne visur prieinami.
Visuomenės sveikatos ir prevencijos implikacijos
Jei molekulinis laikrodis būtų patikimai pritaikytas plačiai populacijai, jis galėtų pakeisti, kaip organizuojama demencijos ankstyvoji diagnostika ir prevencija. Tai leistų prioritetizuoti rizikos valdymą, ankstyvą stebėseną ir įtraukti asmenis į prevencinius programinius arba gyvenimo būdo intervencijas. Tačiau tokia plataus masto taikymo perspektyva reikalauja standartizacijos, prieinamumo užtikrinimo bei lygių galimybių įgyvendinant kraujo biomarkeriais pagrįstą atranką.
Vis dėlto etiniai klausimai išlieka. Ar žmonės norėtų žinoti susiaurintą simptomų atsiradimo laikotarpį, jei gydymo, galinčio sustabdyti progresiją, yra ribotai? Kaip klinikai turėtų komunikuoti tikimybines prognozes, kad nepadarytų psichologinės žalos? Kaip garantuoti duomenų konfidencialumą ir apsaugą nuo galimos diskriminacijos (pvz., draudimo, darbo rinkos)? Šie aspektai nėra vien techniniai; jie reikalauja aiškių sutikimo procedūrų, išsamios konsultavimo infrastruktūros ir viešosios sveikatos politikos planavimo.
Ekspertų įžvalgos
„Tai yra tokio tipo translacinis pažangumas, kurio tikimės — jungtis tarp laboratorinių žymenų ir praktiško sprendimų priėmimo,“ sako dr. Maya Chen, neuroepidemiologė, nesusijusi su tyrimu. „Jeigu bus patvirtinta įvairiose populiacijose, kraujo laikrodis galėtų pakeisti, kaip atrenkame dalyvius į tyrimus ir kaip klinikai prioritetizuoja stebėseną. Tačiau tai privalo būti derinama su tvirtais konsultavimo ištekliais; žinojimas apie laikotarpį be aiškių prevencinių galimybių gali padaryti daugiau žalos nei naudos.“
Tyrimas paskelbtas Nature Medicine ir jį vadovauja Vašingtono universiteto neurologai, tarp jų Suzanne Schindler, kuri pabrėžia prieinamumą: kraujo testai gali išplėsti tyrimų ir klinikų pasiekiamumą už centrų, galinčių atlikti PET skenavimą ar likvoro punkciją, ribų. Kiti artimiausi žingsniai apima modelio testavimą didesnėse ir labiau išsklaidytose kohortose, papildomų kraujo biomarkerių integraciją ir algoritmų tobulinimą, siekiant pagerinti individualų lygį ir nuspėjamumo tikslumą.
Kiti biomarkeriai ir multimodaliniai metodai
Plėtra link klinikinės naudos greičiausiai apims biomarkerų rinkinį: be p‑tau217, NfL (neurofilamento lengvoji grandinė) gali rodyti bendrą neurodegeneracijos laipsnį, amyloid‑beta 42/40 santykis prideda prie amyloidinės patologijos vertinimo, o genetiniai rodikliai (pvz., APOE ε4 genotipas) suteikia papildomą rizikos kontekstą. Kartu su pažangiais mašininio mokymosi modeliais tokie duomenys gali pagerinti prognozių tikslumą ir individualizaciją.
Reguliaciniai ir klinikiniai iššūkiai
Norint integruoti tokią priemonę į klinikinę praktiką reikia ne tik techninės validacijos, bet ir reguliacinio pripažinimo bei aiškių klinikinių gairių, kada ir kam testas turėtų būti skiriamas. Be to, būtina parengti mokymo programas gydytojams ir konsultantams, kad jie galėtų tinkamai paaiškinti rezultatų reikšmę pacientams ir šeimoms.
Išvados ir tolimesni žingsniai
Šiuo metu molekulinis laikrodis yra mažiau asmeninis horoskopas ir labiau mokslinė priemonė — instrumentas, kuris žada patikslinti klinikinių tyrimų laiko planavimą ir pagilinti mūsų supratimą apie lėtą, metų metus trunkantį poslinkį į Alzheimerio ligą. Viltis yra tokia, kad geresnis laiko nustatymas paspartins efektyvesnių gydymo būdų atradimą ir vieną dieną suteiks žmonėms aiškesnį supratimą, ko tikėtis ir kada imtis veiksmų.
Ateityje svarbiausia bus: platesnė validacija įvairiose demografinėse grupėse; integracija su kitais kraujo ir neurovaizdavimo žymenimis; algoritmų patikslinimas siekiant didesnio individualaus tikslumo; ir etinių bei teisiškai apsaugotų komunikacijos praktikų sukūrimas. Tik tada p‑tau217 pagrįstas molekulinis laikrodis galės saugiai pereiti iš pažangios tyrimų priemonės į atsakingai taikomą klinikinį instrumentą, turintį realią vertę pacientams ir visuomenei.
Trumpai tariant: p‑tau217 kraujyje — perspektyvus biomarkeris ir svarbi dalis kuriamo molekulinio laikrodžio. Jo stiprybė — sugebėjimas suteikti laiką ir kontekstą ilgam, lėtai vystančiam procesui, kokiu yra Alzheimerio ligos patofiziologija. Bet kol kas tai labiau įrankis tyrėjams ir klinikiniams tyrimams nei galutinis asmeninis pranešimas pacientui apie ateitį.
Šaltinis: sciencealert

Palikite komentarą