7 Minutės
Pagalvokite apie makrofagus kaip apie kūno tvarkytojų komandą: jie pašalina šiukšles, perdirba svarbias medžiagas ir tyliai reguliuoja organų veiklą. Bet kas moko tą komandą? Nauji tyrimai rodo vieną genetinį reguliatorių, kuris pateikia šiems ląstelėms jų veikimo scenarijų.
Tyrėjai nustatė, kad genetinis faktorius, vadinamas MafB, veikia kaip pagrindinis jungiklis, suteikiantis makrofagams tapatybę ir gebėjimą saugoti organus. Be jo šios svarbios imuninės ląstelės negali pilnai subręsti — vyksta sutrikimai nuo geležies perdirbimo iki plaučių ir inkstų funkcijos.
Nuo monocito iki subrendusio makrofago: MafB posūkis
Po mikroskopu brandinimas primena choreografiją. Kraujyje cirkuliuojantys monocitai patenka į audinius ir, priklausomai nuo vietinių signalų, įgyja specializuotas funkcijas. MafB, kaip transkripcijos faktorius, nuosekliai didina savo ekspresiją per šį perėjimą. Jis neveikia vienas. MafB koordinuoja platų genetinį programų paketą, kuris įjungia genus, reikalingus fagocitozei, atliekų pašalinimui ir audinių palaikymui. Pašalinus MafB, dauguma tų jungiklių niekada neįsijungia. Ląstelės užstringa limbo būsenoje: jos egzistuoja, bet nėra tinkamai paruoštos atlikti savo užduočių.
Tokia limbo būsena turi pasekmių. Liège universiteto Imunofiziologijos laboratorijos vadovaujamose eksperimentuose ląstelės, neturinčios MafB, atrodė morfologiškai nesubrendusios — apvalesnės, mažiau šakojuotos ir funkcionaliai silpnos. Tai patvirtino morfologinius ir funkcinio aktyvumo tyrimus, įskaitant fagocitozės testus, receptorių ekspresijos analizę ir citokinų gamybos matavimus.
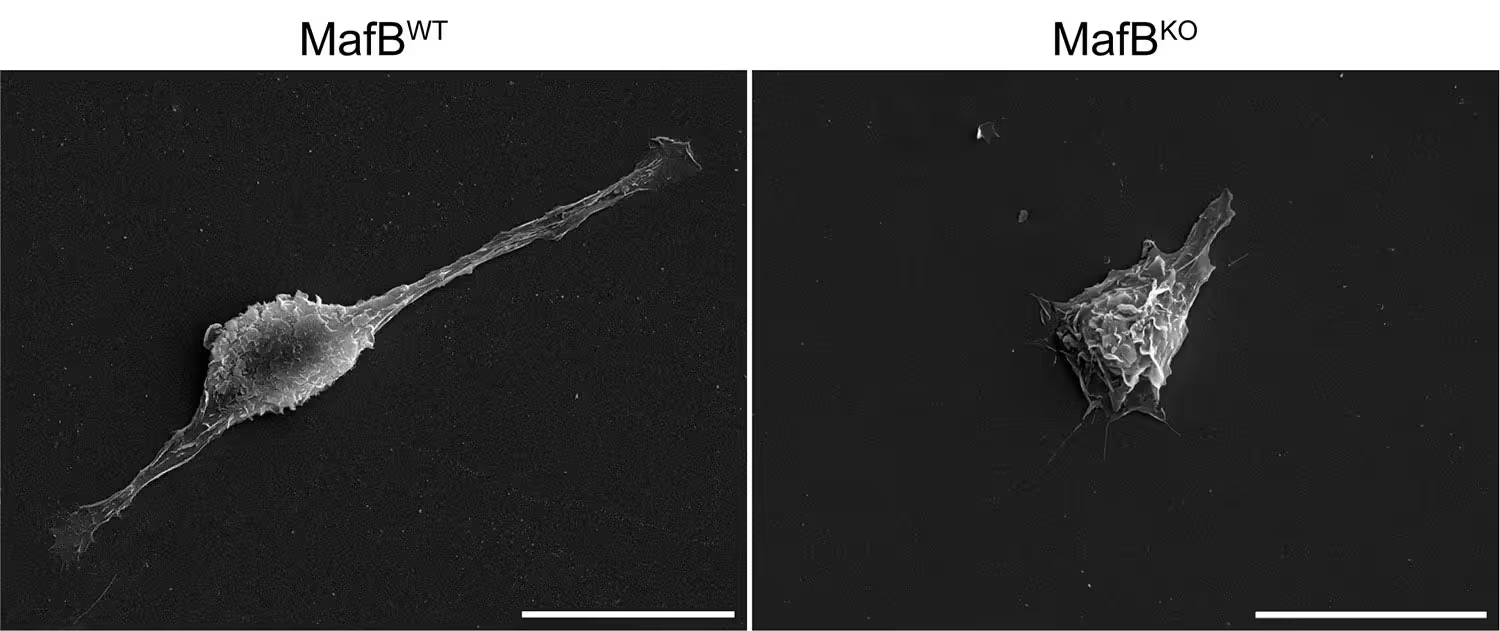
Makrofagai su MafB (WT) atrodo subrendę ir geros formos, tuo tarpu be MafB (KO) jie atrodo apvalūs ir menkai išvystyti.
Kodėl tai svarbu? Nes makrofagai atlieka daugiau nei tik kovą su infekcijomis. Jie perneša geležį iš senstančių raudonųjų kraujo kūnelių, pertvarko tarpląstelinį matricą ir siunčia metabolinius signalus, kurie palaiko plaučių, inkstų, žarnyno ir blužnies pusiausvyrą. Globalus reguliatorius, kaip MafB, suteikia saugomą tapatybę, kad makrofagai galėtų prisitaikyti lokaliai, išlaikant pagrindines funkcijas skirtinguose audiniuose ir rūšyse.
Evoliucinis išsaugojimas ir sisteminės pasekmės
Kuo giliau nagrinėjate DNR, tuo aiškesnis tampa modelis. MafB valdo genų tinklą, aptinkamą pelėse ir žmonėse, o jų pėdsakai matomi ir kitose stuburinių grupėse. Toks evoliucinis išsaugojimas rodo biologinį principą: organizmas naudoja bendrą genetinę programą, kad sukurtų patikimus ląstelių „vaidmenis“ ten, kur jų reikia.
Kai ši programa žlunga, bangavimo efektai pasireiškia kaip organų funkcijos sutrikimai. Liège komanda dokumentavo sutrikusį geležies perdirbimą blužnyje ir subtilius, bet matomus plaučių, žarnyno bei inkstų funkcijos pokyčius, kai makrofagų brendimas buvo užstrigęs. Šie organų lygio rodmenys pateikia svarbią išvadą: imuninės ląstelės tapatybė formuoja fiziologiją, neapsiribodama vien tik patogenų kontrole.
Yra ir klinikinė perspektyva. Lėtinės ligos, tokios kaip fibrozė, nuolatinė uždegiminė būklė, metaboliniai sutrikimai ir kai kurios infekcijos turi makrofagų disfunkciją savo šerdyje. Jei MafB arba jo svarbūs pogrindiniai keliai būtų moduliuojami, mokslininkai galėtų atkurti makrofagų kompetenciją ir taip pagerinti audinių regeneraciją bei homeostazę. Tai ilgas kelias, tačiau su aiškiu molekuliniu orientyru.
Metodai ir įrodymai
Rezultatai paremtas genetiniais modeliais, vienaląsteline profilaktika (single-cell profiling) ir lyginamąja genomika. Stebint MafB ekspresiją, kai monocitai virsta audiniuose rezidentiniais makrofagais, buvo pastebimas pastovus brėžinys: MafB padidėjimas koreliavo su fagocitozės genų ir kitų funkcinį aktyvumą žyminčių žymenų įsijungimu. Nuostolio funkcijai (loss-of-function) tyrimai pateikė ryškiausius duomenis: gyvūnai, neturintys MafB mieloidinėse linijose, turėjo makrofagus, kurie nesugebėjo atlikti daugelio esminių užduočių, o šie trūkumai pasireiškė matomais organų fiziologijos pokyčiais.
Tyrimų metodai apėmė šiuos požiūrius, kurie suteikia mechanistinį ir diagnostinį supratimą:
- Genetiniai modeliai: ląstelių tipo specifiniai MafB knock-out ir inducible knock-down modeliai pelėse leidžia atskirti vystymosi laikotarpius ir audinių specifinius efektus.
- Vienaląstelinė RNA-sek (scRNA-seq): identifikavo pereinamąsias ląstelių būsenas ir susiejo gene ekspresiją su funkciniu profiliu.
- ATAC-seq ir ChIP-seq analizės: atskleidė, kaip MafB keičia chromatino prieinamumą ir tiesiogiai reguliuoja tikslinius genus, susijusius su fagocitoze, receptorų sinteze ir metabolizmu.
- Funkciniai testai in vitro ir in vivo: fagocitozės, citokinų gamybos, geležies perdirbimo ir audinių remonto modeliai parodė fiziologinį poveikį.
Šie pokyčiai nėra abstraktūs. Geležies perdirbimo defektai gali pakeisti sisteminę geležies homeostazę ir prisidėti prie lėtinės ligos anemijos. Plaučių ir inkstų sutrikimai gali padidinti audinių jautrumą traumai ir uždegimui. Trumpai tariant, MafB vaidmuo jungia ląstelių biologiją su viso kūno sveikata.
Terapinės pasekmės ir ateities tyrimai
Taikytis į pagrindinį reguliatorių yra viliojanti idėja, bet ji reikalauja didelio atsargumo. Transkripcijos faktoriai kaip MafB yra daugelio genų programų centre; jų modifikavimas gali turėti plataus spektro poveikį. Labiau tikėtinas trumpalaikis kelias susijęs su pogrindiniais efektais — tais genais ir signalų keliais, kuriuos MafB valdo ir kuriuos galima „vaistinti" ar moduliuoti audinio specifiškai.
Galimos strategijos:
- Downstream terapija: identifikuoti MafB tiesioginius taikinius (pvz., fagocitozės receptorius, geležies transporterius) ir kurti mažųjų molekulių ar biologinių priemonių moduliatorius.
- Audinių specifiškas pristatymas: nanopartikulių ar vektorių naudojimas, kad pakeitimai pasiektų tik tam tikrus audinius (plaučius, inkstus, blužnį), sumažinant sisteminius šalutinius efektus.
- Celėmis grįsta terapija: programuoti makrofagus ex vivo į subrendusią, aukšto MafB lygio būseną ir vėl įvesti juos į pažeistus audinius, taip atstatant jų remonto ir homeostazės funkcijas.
- Genų redagavimas: CRISPR/Cas pagrįstos priemonės, skirtos atstatyti arba švelniai pritaikyti MafB reguliaciją tam tikrose mieloidinėse linijose.
Kokie klausimai lieka? Daugybė. Kaip vietiniai audinių signalai sąveikauja su MafB, kad sukurtų tokią įmantrią makrofagų fenotipų įvairovę? Ar dalinis MafB programų atkūrimas gali išgelbėti organų funkciją ligos modeliuose? Ar aplinkos arba metabolinis stresas gali trikdyti šią programą taip, kad spartintų lėtines ligas? Šie klausimai remia tiek fundamentinius mokslinius, tiek transliacinius tyrimus.
Eksperto įžvalga
Dr. Eleanor Voss, imunologė ir transliacinė tyrėja, pastebi: "MafB reiškia svertą tarp tapatybės ir veiksmo. Mes ilgai žinojome, kad makrofagai prisitaiko prie vietinių nišų; dabar matome išsaugotą genetinį pagrindą, kuris padaro tą prisitaikymą patikimą. Terapiniu požiūriu iššūkis yra gerbti tą pagrindą, tuo pat metu selektyviai reguliuojant jo išvestis. Tai yra precizinė biologija veiksmui."
Supratimas, kaip vienas transkripcijos faktorius gali koordinuoti tokias plačias ląstelines atsakomybes, perrėžia mūsų požiūrį į imuninę sistemą. Tai nėra pavieniai, laisvi gynėjai — tai yra programuoti prižiūrėtojai. Dabar svarbiausias klausimas: kaip paversti tą programavimą gydymo strategijomis, kurios išsaugo funkciją neardydamos kruopščiai evoliucijos suformuotą tinklą?
Papildomi techniniai pastebėjimai ir praktiniai patarimai mokslininkams
Tyrėjams, dirbantiems su MafB, verta apsvarstyti kelis praktinius aspektus:
- Laiko dinamika: MafB ekspresija nėra staigi „įjungimo/išjungimo" funkcija — dažnai ji palaipsniui didėja per išsivystymą, todėl laiko taškų tyrimai (time-course) yra būtini.
- Audinių specifika: vienaląstelinis atlasas padeda atskirti, kurie vietiniai signalai lemia MafB priklausomus fenotipus kiekviename audinyje.
- Kompenzacijos mechanizmai: kitų MAF šeimos narių aktyvumas gali kompensuoti MafB netektį, todėl reikia tirti šių šeimos genų tinklo tinkamumą.
- Biomarkeriai: identifikuoti patikimus funkcinės brandos žymenis, kuriuos galima panaudoti diagnostikoje ir terapijos stebėjimui.
Visa tai rodo, kad tolesni tyrimai turėtų derinti fundamentinius mechanistinius eksperimentus su translaciniais modeliais, siekiant saugaus ir veiksmingo farmakologinio ar ląstelėmis pagrįsto poveikio.
Išvados
MafB veikia kaip centrinis taškas, kuriame susijungia ląstelių tapatybė ir funkcija. Jo vaidmuo makrofagų brandinime atveria naujas biologijos ir medicinos galimybes: nuo supratimo, kaip formuojasi audinių homeostazė, iki potencialių terapinių taikų lėtinėms ligoms gydyti. Nors tiesioginis transkripcijos faktoriaus moduliavimas reikalauja atsargumo, atkuriant MafB valdomas programas arba taikant jų pogrupius galima pasiekti konkretesnę ir saugesnę terapiją. Ateities darbai, derindami genų reguliavimo tyrimus, vienaląstelinę biologiją ir audinių specifiškas terapijas, turėtų patikslinti, kaip geriausiai versti šią gairę į gydymo strategijas.
Šaltinis: scitechdaily

Palikite komentarą