8 Minutės
Kažkas labai smulkaus nutraukė mirtiną susiėjimą tarp baltymų neuronų viduje. Pasekmė: mitochondrijos — ląstelės galios stotys — pradėjo gesti, o neuronai, kurie anksčiau veikė aktyviai, ėmė silpti. Šis dviejų reiškinių poravimasis yra centras naujoje Case Western Reserve University School of Medicine studijoje, kuri atseka tiesioginį kelią nuo alfa-sinukleino sankaupų iki mitochondrijų sutrikimo ir siūlo molekulinį masalą, galintį sustabdyti žalą.
Alfa-sinukleinas jau dešimtmečius yra įtariamas Parkinsono ligos veiksnys. Kai jis neteisingai sulankstomas ir agreguoja, neuronai kenčia. Nepriklausomai nuo to, klinicistai ir laboratorijų mokslininkai pastebėjo, kad paveiktų neuronų mitochondrijos yra silpnos, energijos stokojančios ir linkusios inicijuoti ląstelių mirtį. Tačiau kaip šie du reiškiniai susijungia, iki šiol buvo neaišku. Naujas tyrimas išryškina tikslų biocheminį tarpusavio ryšį: alfa-sinukleinas prisijungia prie fermento giliai mitochondrijose, vadinamo ClpP, ir ši sąveika, atrodo, sutrumpina organelės gebėjimą tvarkyti pažeistus baltymus bei palaikyti metabolinį balansą.
Ko komanda atrado ir kaip tai tikrino
Tyrėjai naudojo įvairius modelius: ex vivo žmogaus smegenų audinį, in vitro audinių kultūras su išaugintais neuronais ir gyvūnų modelius (pelėse). Jie stebėjo, kaip alfa-sinukleinas prisitvirtina prie mitochondrijinio ClpP fermento ir užfiksavo tolesnį mitochondrijų baltymų kokybės kontrolės sutrikimą. Galima įsivaizduoti ClpP kaip atliekų surinkimo sistemą jėgainėje: jei ji užblokuojama, atliekos kaupiasi, o variklis pradeda klibėti.
Eksperimentiniai metodai ir rodikliai
Tyrime buvo taikomi keli techniniai metodai, skirti patvirtinti alfa-sinukleino–ClpP sąveiką ir jos pasekmes:
- Baltymų susiejimo ir koimunoprecipitacijos (co-IP) tyrimai, patvirtinantys tiesioginį alfa-sinukleino ir ClpP fizinį prisijungimą.
- Mitochondrijų funkcijos matavimai — ATP gamybos analizė, membranos potencialo tyrimai (pvz., JC-1 dažymas), kvėpavimo grandinės aktyvumo vertinimas per oksidacinio fosforilinimo (OXPHOS) matavimus.
- Baltymų kokybės kontrolės indikatoriai — padidėjęs užsilikusių arba nesuardytų baltymų kiekis, padidinta oksidacinė žala ir sumažėjusi proteazominė bei mitofagijos veikla.
- Uždegimo žymenys — citokinų (pvz., TNF-α, IL-1β) ir glijų aktyvacijos rodiklių nustatymas audiniuose.
- Funkciniai gyvūnų testai — motorinių sugebėjimų (rotarod, open field) ir kognityvinių gebėjimų (Morris vandens labirintas ar panašūs testai) vertinimas pelėms.
Šių rodiklių visuma leido tyrėjams suformuluoti priežastinę grandinę: alfa-sinukleino prisijungimas prie ClpP sutrikdo baltymų šalinimą mitochondrijose, kas veda prie energijos krizių, neurodegeneracijos ir klinikinių Parkinsono simptomų stiprėjimo.
CS2 — decoy (masalo) peptidas kaip terapinis priedas
Užuot puolę alfa-sinukleino visuotiniam sumažinimui (kas gali būti sudėtinga ir turėti šalutinių efektų), tyrėjai sukūrė trumpą peptidą, pavadintą CS2, kuris veikia kaip decoy ar masalas. Pagrindinė idėja yra paprasta: nukreipti „kliūtį“ taip, kad alfa-sinukleinas prisirištų prie CS2, o ne prie ClpP, tad mitochondrijos galėtų tęsti baltymų tvarkymą ir išlaikyti metabolinį stabilumą.
Bandymų rezultatai parodė, kad CS2:
- mažina uždegimo žymenis ex vivo žmogaus smegenų audiniuose;
- išlaiko mitochondrijų aktyvumą kultivuotuose neuronuose (geri ATP lygiai, stabilus membranos potencialas);
- pelėms suteikia matomų pagerėjimų motoriniuose ir kognityviniuose testuose, palyginti su kontroline grupe;
- apsaugo ClpP fermento funkciją, mažina mitochondrijinį baltymų kaupimąsi.
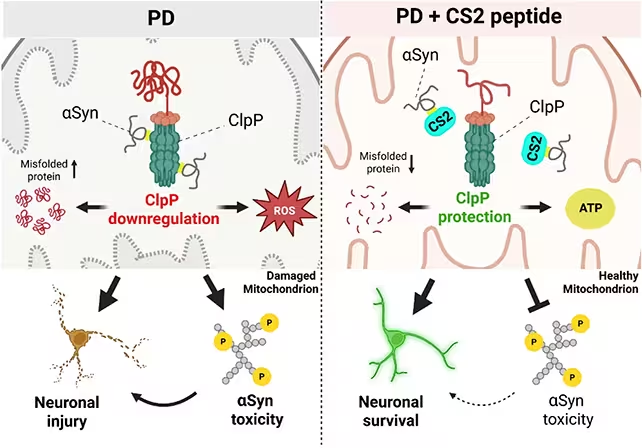
Buvo parodyta, kad CS2 apsaugo ClpP fermentą.
Tokia apsauginė priemonė yra reikšminga, nes ji nukreipta į mechanistinį žingsnį, kuris, manoma, yra ankstyvas daugelio Parkinsono ląstelių sutrikimų pražangos momentas. Jei alfa-sinukleino sąveika su ClpP yra vienas iš ankstyvųjų ligos nuokrypių, tuomet ClpP apsauga galėtų sustabdyti arba sulėtinti kelis vėlesnius žalojimus.
Mokslinis kontekstas ir pasekmės
Parkinsono liga nėra vieno kelio sutrikimas. Genetiniai faktoriai, aplinkos veiksniai, senėjimas ir ląstelių stresas susipina sudėtingais būdais. Naujas tyrimas nepateikia universalaus išgydymo pažado, tačiau jis suteikia aiškumą: apibrėžiama molekulinė kontaktinė vieta, kurią galima modifikuoti. Intervencija šioje grandinėje galėtų būti derinama su kitomis strategijomis — sumažinti alfa-sinukleino agregaciją, skatinti mitochondrijų biogenezę arba reguliuoti uždegimą.
Biologinis svarbumas ir platesnės implikacijos
Atkurdami ClpP veiklą arba apsaugodami jį nuo alfa-sinukleino prisijungimo, tyrėjai atveria kelią kelioms terapinėms kryptims:
- Tiesioginės apsaugos strategijos — peptidai tipo CS2 ar mažos molekulės, kurios konkurencingai blokuoja alfa-sinukleino prisijungimą prie ClpP.
- Komplementarinės priemonės — jungtinės terapijos, kurios tuo pačiu metu mažina alfa-sinukleino agregaciją (pvz., antikūnai ar chelatai), stiprina mitofagiją arba stiprina antioksidacines sistemas mitochondrijose.
- Transporto sprendimai — efektyvesni CNS tiekimo metodai, leidžiantys peptidams pasiekti pažeistus neuronus per hematoencefalinį barjerą.
Vis dėlto reikšmingas įspėjimas: bet koks molekulinis modifikavimas, keičiantis baltymų sąveikas mitochondrijose, turi būti kruopščiai patikrintas dėl netikėtų nepageidaujamų poveikių. Mitochondrijų kokybės kontrolės sistemos yra subtiliai subalansuotos; net nedideli pokyčiai gali turėti pločiu poveikiu į ląstelių metabolizmą ir organizmo homeostazę.
Laikotarpis iki klinikinių tyrimų ir reguliavimo iššūkiai
Tyrėjų komanda numato maždaug penkerių metų ruožą iki CS2 ar panašių biologinių preparatų pirmųjų žmogaus tyrimų. Tai yra realistiškas terminas peptidinei terapijai, atsižvelgiant į papildomus stabilumo, farmakokinetikos, toksiškumo ir tiekimo sprendimus, kuriuos reikia įrodyti preklininiuose tyrimuose.
Keli esminiai iššūkiai:
- Peptido stabilumas organizme — natūralūs peptidai greitai skaidomi proteazėmis; reikės modifikuotų analogų arba formulavimo, kurie didintų biologinį prailginimą.
- Hematoencefalinio barjero perėjimas — pasiekti pakankamą koncentraciją tose smegenų srityse, kurioje vyksta alfa-sinukleino agregacija, yra kritinis uždavinys.
- Off-target (nepageidaujami) efektai — reikia įrodyti, kad CS2 nesikiša į kitų mitochondrijų fermentų veikimą ar kitų ląstelių kokybės kontrolės mechanizmų funkcijas.
- Ilgalaikė sauga — chroniniai tyrimai rodys, ar ilgalaikis ClpP modulavimas turi saugių profilių gyvūnų modeliuose prieš pereinant prie žmonių.
Jeigu šie klausimai bus adresuoti sėkmingai, CS2 arba jos palyginami analogai gali papildyti esamų Parkinsono terapijų arsenalą, orientuotą ne tik į simptomų slopinimą, bet ir į ląstelių energetikos išsaugojimą.
Eksperto įžvalga
"Šis darbas yra reta mechanistinio tikslumo ir terapinio išradingumo kombinacija," sako daktarė Elaine Ramirez, fiktyvi neurobiologė, tirianti mitochondrijų dinamiką. "Sukurti masalą, kuris perima patogeninį baltymą mitochondrijų slenksčio vietoje, yra gudru. Ateities iššūkis — pateikimas: kaip patikimai tiekti pakankamą peptido kiekį į pažeidžiamus neuronus nepažeidžiant kitų ląstelių kokybės kontrolės sistemų."
Straipsnis publikuotas žurnale Molecular Neurodegeneration ir atveria kelias krypčių: CS2 stabilumo optimizavimas, ilgalaikio saugumo tyrimai ir galimybė, kad panašūs «masalai» galėtų apsaugoti ir kitus mitochondrijų fermentus. Jis taip pat užduoda platesnį klausimą: jei pavyks užkirsti kelią mitochondrijų energijos praradimui, ar galime pakeisti Parkinsono ligos trajektoriją nuo neišvengiamo progresavimo į valdomą būklę arba net sustabdyti jos vystymąsi? Ateities eksperimentai bus lemiami, bet šiuo metu tyrimų lauke atsirado naujas, aiškus taikinys, kurį verta sekti.
Techninės detalės ir tolesni moksliniai žingsniai
Norint užtikrinti, kad CS2 ar panašios molekulės būtų tinkamai išvystytos, reikės šių žingsnių:
- Medicininiai chemijos žingsniai peptido modifikavimui: įskaitant D-amino rūgščių įterpimą, N-termino acetilinimą ar PEGilinimą, siekiant padidinti inkstų filtracijos ir proteazių atsparumą.
- Farmakodinamikos ir farmakokinetikos studijos įvairių administravimo kelių (intraveninis, intratekalinis, nosinis, nanopartikulinis pristatymas) efektyvumo nustatymui.
- Plėtojant biomarkerius: aiškūs molekuliniai žymenys, kurie leistų matuoti CS2 poveikį pacientams (pvz., sumažėję uždegimo rodikliai, atstatyta ATP gamyba ar mažesnės alfa-sinukleino agregacijos dalys likvoruose ar kraujyje).
- Tikslesni genetinių Parkinsono formų modeliai: ar CS2 veikia tiek sporadines, tiek paveldimas alfa-sinukleino susijusias formas?
Visi šie papildomi tyrimai prisidės prie to, kad CS2 būtų įvertintas kaip galimas kandidatas į ankstyvos fazės žmogaus tyrimus.
Reikšmė pacientams ir šeimoms
Nors tai yra dar agrarinis mokslinis žingsnis, atradimas turi realią prasmę žmonėms, gyvenantiems su Parkinsono liga. Terapijos, kurios išsaugo neuronų energetinę veiklą, galėtų reikšti ilgesnį savarankišką funkcionavimą, lėtesnį motorinių ir kognityvinių funkcijų blogėjimą bei geresnę gyvenimo kokybę. Net jei CS2 netaps visuotine panacėja, jos principas — nukreipti ir apsaugoti mitochondrijų baltymų valdymo mechanizmus — gali tapti vertingu papildymu kitoms gydymo strategijoms.
Apibendrinant, tyrimas suteikia naują molekulinį langą į Parkinsono ligos patogenezę ir pateikia pragmatišką, tikslinę terapinę idėją. Ateities darbai, skirti galutiniam saugumo, efektyvumo ir pristatymo sprendimui, bus lemiami, tačiau dabartiniai rezultatai suteikia pagrįstą optimizmą ir naują krypčių sąrašą neurodegeneracinių ligų tyrimams.
Šaltinis: sciencealert


Palikite komentarą