8 Minutės
Tyrėjai praneša apie mažą, inžinerinį peptidą, kuris išlaiko Parkinsono ligai susijusį baltymą alfa-sinukleiną jo natūralioje konformacijoje, taip užkertant kelią neteisingam sulipimui ir agregacijai, kurie, manoma, pažeidžia neuronus. Molekulė išbandyta paprastoje žarnelio (worms) modelio sistemoje: ji atspari ląsteliniam suirimui, nesutrikdo alfa-sinukleino fiziologinių funkcijų neurotransmisijoje ir siūlo ankstyvos stadijos, prevencinę strategiją stabdant baltymų agregaciją, kol ji dar nėra toksiška.
Mažas peptidas, užrakinantis alfa-sinukleiną vietoje
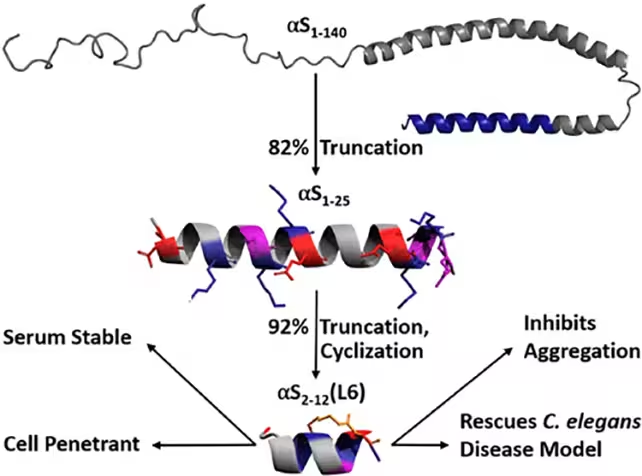
Alfa-sinukleinas yra nedidelis neuroninis baltymas, dalyvaujantis dopamino ir kitų neurotransmiterių reguliavime. Parkinsono ligos ir susijusių sutrikimų atveju šis baltymas gali neteisingai sulinkti (misfolding) ir susidaryti netirpius agregatus, kurie trukdo neurų tarpusavio ryšiams ir ilgainiui prisideda prie ląstelių mirties. Vietoje bandymų ištirpdyti jau susidariusius guotus, Bato universiteto vadovaujama tyrėjų komanda sukūrė peptidą, kuris prisijungia prie alfa-sinukleino ir stabilizuoja jo sveiką konformaciją — iš esmės „užšaldydamas“ baltymą prieš jam įgaunant kenksmingą formą.
Pradinis požiūris remėsi didesniu alfa-sinukleino fragmentu, anksčiau įrodyta sumažinančiu agregaciją. Iš to fragmento mokslininkai iškirpo minimalų aktyvų sekos ruožą ir cheminiu būdu sustiprino jį naudojant laktaminius tiltelius (lactam bridges) — struktūrines kilpas, kurios fiksuoja peptido formą ir reikšmingai pagerina jo atsparumą ląsteliniam skaidymuisi. Tokie cheminiai modifikavimai daro peptidą mažiau pažeidžiamą proteazėms ir prailgina jo biologinį stabilumą, kas ypač svarbu viduląstelinių taikinių atveju.
Žarnelių (Caenorhabditis elegans) modeliuose, imituojančiuose Parkinsono ligos patofiziologiją, šis inžinerinis peptidas užkirto alfa-sinukleino neteisingam sulinkimui, sumažino toksiškų agregatų susidarymą ir tai padarė be pastebimos ląstelinės toksikologijos. Tokie rezultatai pabrėžia strategiją, kuri ne naikina jau susiformavusių guotų, o blokuoja pirminį etapą — monomerų arba pradinių oligomerų perėjimą į patologines struktūras.
Pritaikant tokį metodą svarbu užtikrinti, kad peptidas būtų selektyvus ir neveiktų kitų reikšmingų baltymų ar jų funkcijų. Šio tyrimo atveju peptidas išlaikė alfa-sinukleino fiziologinį vaidmenį sinapsinėse funkcijose, kas yra pagrindinis reikalavimas bet kuriai terapijai, nukreiptai į gausiai paplitusius ir normaliai veikiančius neirobiologinius baltymus.
Kodėl neteisingo sulinkimo prevencija svarbi ligos atžvilgiu
Yra esminis skirtumas tarp gydymo strategijų, kurios pašalina jau susidariusius agregatus, ir tų, kurios blokuoja jų susidarymą. Agregatai gali būti tiek ligos pasekmė, tiek aktyvus jos progresavimo veiksnys; atskirti priežastį nuo pasekmės — vienas didžiausių iššūkių neurodegeneracijos tyrimuose. Prevencinės molekulės, tokios kaip aptariamas peptidas, orientuojasi į ankstyviausią agregacijos kaskadės įvykį: pradinį neteisingą sulinkimą (misfolding), kuris dažnai yra reikšmingas impulso taškas tolesnei patologijai.
Neteisingas alfa-sinukleino sulinkimas gali inicijuoti oligomerų formavimąsi — mažų, dinamiškų kompleksų, kurie gali būti ypač toksiški neurams. Šios oligomerinės formos gali trikdyti membranų vientisumą, ionų kanalų veiklą ar mitochondrijų funkciją, taip pat gali skatinti uždegimines reakcijas. Blokuojant šį pradinį etapą, galima sumažinti tiek lokalią, tiek sisteminę ląstelių žalą, o tai reiškia potencialią ligos progresavimo sulėtėjimą arba prevenciją asmenims, kuriems yra didesnė rizika.
Prevencinė strategija yra ypač perspektyvi tiems, kurie identifikuojami kaip padidintos rizikos grupė — pvz., turint genetinius pakitimus (LRRK2, GBA mutacijos) arba ankstyvus biomarkerius, rodančius alfa-sinukleino patologiją. Nukreipimas į natūralią baltymo konformaciją gali išsaugoti normalų neurotransmiterių reguliavimą ir tuo pačiu sumažinti kenkėjiškų agregatų kaupimąsi. Tokia sinukleino stabilizavimo strategija gali būti laikoma tinkama prevencijos priemone arba ankstyvuoju intervenciniu gydymu.
Tokia prevencinė perspektyva taip pat svarbi platesniame neurodegeneracinių ligų kontekste. Lewy kūnelių demencija ir Alzheimerio liga, kaip ir Parkinsono liga, dalinasi kai kuriais baltymų agregacijos mechanizmais; stabilizuojant natūralias baltymų konformacijas, galima plėsti taikymą į įvairias baltymų agregacijos sutrikimų formas. Be to, ankstyva intervencija, grindžiama genetine ar biologine rizikos identifikacija, suteikia galimybę pasiekti pacientus dar prieš prasidedant plačiai patologinei grandinei.
Labai svarbu, kad bet kuri prevencinė priemonė išliktų neutralia esminėms fiziologinėms funkcijoms: alfa-sinukleinas atlieka svarbų vaidmenį sinapsinėje pakuotėje ir neurotransmiterių apdorojime, todėl selektyvumas yra būtinas. Bato universiteto komanda pažymi, kad peptidas veikia gyvuose organizmuose ir nesutrikdo alfa-sinukleino fiziologinės rolės — tai yra lemiamas reikalavimas kuriant terapijas, skirtas gausiai paplitusiems baltymams.
Tiekimo (delivery) iššūkiai, platesnės implikacijos ir tolimesnės kryptys
Nors rezultatai žarnelių modeliuose yra viltingi, perkelti ląstelėje stabilų peptidą į žmogui tinkamą terapiją reiškia kelis esminius iššūkius. Peptidai kraujotakoje gali būti greitai pašalinami inkstais ar degraduojami plazmos proteazėmis; jie taip pat sunkiai praeina per hematoencefalinį barjerą (blood–brain barrier, BBB) ir gali būti atpažįstami bei neutralizuojami imuninio atsako. Tyrimas Bato universitete cheminiu būdu sprendė viduląstelinio stabilumo problemą, tačiau saugus ir efektyvus molekulės pristatymas į žmogaus smegenų audinį lieka didelis inžinerinis ir farmakologinis iššūkis.
Galimos pristatymo strategijos apima nanodalelių nešiklius, liposomas, modifikuotus peptidus su BBB perpildymo peptidų sekvencijomis arba konjugavimą prie transportinių baltymų, kurie natūraliai pereina per barjerą. Kiekvienas variantas turi savų privalumų ir rizikų: nanodalelės gali pagerinti stabilumą ir padėti taikymui, bet kelia klausimus dėl ilgalaikio saugumo ir atskiro toksikologinio profilio; modifikuoti peptidai, kurie praeina BBB, turi išlikti selektyvūs ir neturėti nepageidaujamo poveikio periferinėms sistemoms.
Imunogeninis atsakas yra dar vienas svarbus aspektas. Net mažas peptido modifikavimas gali sukelti naujų epitonų susidarymą, kuriuos organizmas traktuoja kaip svetimus. Todėl tolimesniuose preklininiuose tyrimuose reikia vertinti ne tik efektyvumą, bet ir galimą imuninį atsaką, įskaitant antikūnų generavimą ir uždegimatinių citokinų profilį.
Tolimesni žingsniai apims bandymus žinduolių modeliuose, pristatymo metodų optimizavimą (pvz., nanopartikulės, modifikuoti peptidai arba vektoriai) ir ilgalaikio saugumo bei veiksmingumo vertinimus. Sėkmės atveju šis peptidas arba jo modifikuotos atmainos galėtų tapti prevencinės terapijos dalimi asmenims, turintiems didelę Parkinsono ligos riziką arba pacientams ankstyvoje ligos stadijoje, kur baltymų agregacija dar nėra plačiai išplitusi.
Tyrėjų komanda ir finansuotojai pabrėžia, kad tai yra ankstyvas, bet svarbus etapas. Julia Dudley iš Alzheimer's Research UK, kuri bendrafinansavo tyrimą, pažymėjo platesnę prasmę: panašios agregacijos procesai lemia Lewy kūnelių demenciją ir Alzheimerio ligą, tad giminingų baltymų konformacijų stabilizavimas gali tapti platesne strategija neurodegeneracinių sutrikimų kontrolei. Straipsnis publikuotas žurnale JACS Au (2025) ir remiasi ankstesniais alfa-sinukleino sąveikos vietų struktūriniais žemėlapiais.
Eksperto įžvalga
„Sukurti peptidą, kuris būtų tiek stabilus ląstelėse, tiek selektyvus ligai jautriai baltymo formai, yra sudėtingas subalansavimo uždavinys,“ sako dr. Mark Ellison, neurochemikas ir mokslo komunikatorius. „Šis tyrimas demonstruoja racionalią projektavimo kryptį, kuri sumažina agregaciją neblokuodama baltymo įprastos funkcijos — būtent tokio specifinio poveikio mums reikia, pereinant nuo modelinių organizmų prie klinikinių tyrimų.“
Praktiniai tolimesni žingsniai bus orientuoti į: pirmiausia – išplėstus preklininius tyrimus žinduoliuose, siekiant patikrinti terapinį langą, dozių dažnį ir ilgalaikį poveikį;
antra, – pristatymo platformų optimizavimą, kad būtų pasiektas smegenų audinys: nanopartikulės, rekombinantinių antikūnų peptidų konjugatai arba receptoriniu tarpu baltymų transportu paremtos strategijos;
trečia, – farmacokinetinių ir imunologinių profilių išaiškinimą, kad būtų sumažintos nepageidaujamos reakcijos ir užtikrintas pakankamas peptido buvimo laikas tikslineje vietoje;
ketvirta, – žmogaus ligos heterogeniškumo įvertinimą: genetinių rizikos veiksnių, biomarkerių ir ligos stadijos įtaką terapijos efektyvumui. Jei šie etapai bus sėkmingi, peptidas arba su juo susijusios molekulės galėtų tapti prevencinės arba ligos modifikuojančios strategijos dalimi asmenims, kurie yra aukštos rizikos Parkinsono ligai ar kitiems baltymų agregacijos sutrikimams.
Šiuo metu tyrimas atstovauja „principo įrodymui“: racionaliai projektuojant mažus peptidus galima sukurti molekules, kurios ląstelėse patruliuoja, blokuoja kenksmingą baltymų agregaciją ir tuo pačiu išsaugo normalią biologiją — tai pažadantis planas naujoms ligas modifikuojančioms priemonėms neurodegeneracijos srityje.
Apibendrinant, alfa-sinukleino stabilizavimo technologija, paremta cheminiu peptidų sustiprinimu, atveria naują kelią prevencinėms terapijoms prieš Parkinsono ligą: tokios terapijos galėtų veikti ankstyvose ligos stadijose arba net kaip profilaktinė apsauga tiems, kurie turi aukštą genetinę ar klinikinę riziką. Tolimesni moksliniai ir inžineriniai sprendimai, ypač susiję su tinkamu pristatymu į smegenis ir imuninio saugumo užtikrinimu, bus lemiami, ar ši koncepcija galės pasiekti klinikinį pritaikomumą ir tapti dalimi Parkinsono ligos gydymo arsenalo.
Šaltinis: sciencealert

Palikite komentarą