7 Minutės
Tyrėjai Ispanijoje identifikavo nedidelę amigdalos neuronų grupę, kuri gali sukelti — ir, atstatant pusiausvyrą, atvirkščiai pakeisti — pelėms būdingą nerimo pobūdžio elgesį. Tikslindami geną GRIK4 ir jo baltymą GluK4, mokslininkų komanda atkūrė normalų socialinį elgesį ir sumažino depresijos požymius pelėms, kurios buvo selektyviai išvystytos kaip jautrios nerimui. Šis atradimas atveria tikslinio poveikio galimybes ateities terapijoms, orientuotoms į konkretus nervinių ląstelių pogrupį ir receptorius, tokiu būdu sumažinant plataus poveikio vaistų šalutinį efektą. Straipsnis publikuotas žurnale iScience (2025) ir atliktas bendradarbiaujant Ispanijos Nacionaliniam tyrimų tarybai (CSIC) bei Miguel Hernández universitetui Elče (UMH).
Kaip kelios ląstelės keičia emocinę pusiausvyrą
Tyrimas sutelktas į bazolateralinę amygdalą (BLA) — smegenų sritį, kuri vaidina centrinius vaidmenis baimės apdorojime, sprendimų priėmime ir emocinėje atmintyje. Užuot ieškoję plataus masto, viso smegenų tinklo pokyčių, tyrėjai sekė aktyvumą specifinėje BLA neuronų populiacijoje. Jie nustatė, kad būtent pusiausvyros sutrikimas šioje ribotoje neuronų grupėje buvo pakankamas sukelti patologinį nerimą ir socialinio elgesio trūkumus modeliuose. Tokia išvada pabrėžia, kad loginės vietos — ribotos neuronų sankaupos — gali turėti didelį poveikį elgesiui ir emocijoms, o tai svarbu neurobiologijai ir klinikinei neuropsychiatrijai.
Eksperimentuose, kai buvo perspausdintas (overexpressed) genas GRIK4, padidėjo GluK4 baltymo gamyba šioje neuronų grupėje. Pelės su pakilusiomis GluK4 ekspresijos reikšmėmis vengė atvirų erdvių (open-field test metu), demonstravo socialinį atsitraukimą socialinių sąveikų testuose ir rodė depresijai artimus požymius, pavyzdžiui sumažėjusį motyvaciją ar aktyvumo lygį. Be to, tos pačios pelės turėjo sunkumų objektų atpažinimo užduotyse (novel object recognition), kas leidžia manyti, kad GluK4 disbalansas paveikė platesnį smegenų tinklą už ribos BLA – galimos įtakos apima susijusias hipokampo, prefrontalinės žievės ir sensorinių grandžių funkcijas. Šie elgesio testai — atviro lauko, socialinės sąveikos, objekto atpažinimo ir papildomi kognityviniai matavimai — suteikė nuoseklius duomenis apie GluK4 vaidmenį nerimo ir socialinių deficito fenotipuose.
Genų redagavimas nuramina nerimastingas peles
Koreguoti šiuos elgesio pokyčius tyrėjai naudojo tikslinei smegenų zonai skirtas genų redagavimo priemones, kurios leisdavo sumažinti perteklinę GRIK4 kopijų ekspresiją būtent BLA. Naudotos metodikos apima molekulinius įrankius, panašius į CRISPR/Cas bazes arba genų modulaciją naudojant specifines vektorių sistemas — tikslas buvo sumažinti GluK4 lygį be plataus poveikio kitiems audiniams. Rezultatas buvo ryškus: nerimui būdingi ir socialinio elgesio deficito požymiai išnyko, o gydytos pelės vėl ėmė rodyti labiau įprastus tyrinėjimo ir sąveikos modelius. Kaip vienas iš tyrimo autorių, neuromokslininkas Álvaro García, pastebėjo: 'Toks paprastas lygio sureguliavimas buvo pakankamas atstatyti nerimą susijusį ir socialinį elgesį — tai iš tiesų įspūdinga.' Šis pastebėjimas patvirtina, kad lokalus molekulinis poveikis vienai baltymų eilutei gali turėti plataus masto elgesio pasekmes, o tai ypač svarbu projektuojant tikslingas terapijas.
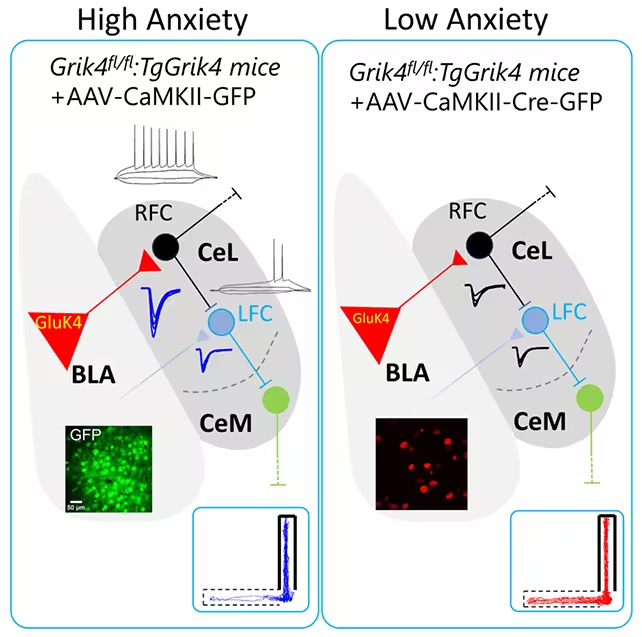
Svarbu pažymėti, kad tokia pat intervencija veikė ir natūraliai didesnį nerimą rodžiusioms negenetiškai modifikuotoms pelėms, kas rodo, jog metodas yra veiksmingas ne tik genetinių inžinerijų modeliuose. Tai sustiprina idėją, kad GRIK4/GluK4 reguliavimas gali būti taikomas plačiau — pavyzdžiui, gyvūnų populiacijose, kur nerimas yra išreikštas fenotipiškai, bet ne sukeltas konkrečios transgeninės manipuliacijos. Tačiau net ir po sėkmingo GRIK4 reguliavimo, gydytoms pelėms išliko problemos objekto atpažinime ir kognityviniuose testuose. Toks rezultatas rodo, kad nerimo sukeliami pažinimo sutrikimai apima papildomas smegenų sritis ar grandis, kurių šios manipuliacijos nepašalino, ir todėl pilnas kognityvinių simptomų atstatymas reikalautų platesnio grandžių supratimo ir galbūt kombinuotų intervencijų.
Kodėl tai svarbu — ir ką dar nežinome
Identifikavus konkrečią neuronų populiaciją, kurios vienintelis aktyvumas gali sukelti patologinį nerimą, keičiama mokslininkų perspektyva, kaip galima gydyti afektinius sutrikimus. Vietinio grandinio taikymas atveria galimybes kurti terapijas, apribojančias poveikį tik tam tikrai smegenų sričiai ar neuronų pogrupiui, o tai teoriškai sumažina bendrinio poveikio vaistų, veikiančių visą smegenų cheminię aplinką, rizikas ir šalutinius efektus. Tokia strategija gali keisti nusistovėjusius požiūrius, kuriuose dažnai siekiama slopinti simptomus sisteminiais neuromoduliatoriais.
Vis dėlto žmogaus pernešimas iš gyvūnų modelių tebėra spekuliatyvus. Nors pelių modeliai yra esminė ankstyvųjų neurobiologinių mechanizmų tyrimų dalis, žmogaus smegenys yra struktūriškai ir funkcionaliai sudėtingesnės, o amigdala žmonėms integruojasi į platesnius sociokultūrinius bei kognityvinius kontekstus. 'Jau žinojome, kad amigdala dalyvauja nerime ir baimėje, tačiau dabar identifikavome specifinę neuronų populiaciją, kurios disbalansas vienas pats gali inicijuoti patologinį elgesį,' sakė Juan Merma, vienas iš straipsnio bendraautorių. Kitas tyrėjas, Lerma, pabrėžė, kad tokių grandžių taikymas galėtų tapti 'efektyvia ir labiau lokalizuota strategija gydyti afektinius sutrikimus'. Tačiau abejonių kelia translacija į kliniką: reikia įvertinti saugumą, ilgalaikį poveikį, galimus kompensacinius tinklo pokyčius ir etiškumo bei reguliavimo aspektus, susijusius su smegenų genų modifikavimu.
Ateities kryptys ir terapinės perspektyvos
Tolesni žingsniai apima išsamų žemėlapio sudarymą, kaip GluK4 disreguliacija pakeičia susijusius smegenų grandis už BLA ribų — įskaitant hipokampą, priekines žievės sritis ir monoaminergines sistemas — bei eksperimentinius bandymus, siekiant rasti saugius ir veiksmingus GRIK4 moduliavimo pristatymo būdus didesniems gyvūnams. Svarbios temos: vektorių saugumas ir tikslingumas, imuninės reakcijos į virusinius žmones primenančius vektorius, galimi off‑target efektai CRISPR tipo sistemose, bei baltymų reguliavimo trukmė. Tokie bandymai suteiks duomenų apie dozavimą, laiko langus ir grįžtamojo ryšio mechanizmus, kurie reikalingi planuojant saugius bandymus žmonėms.
Metodikos, naudojamos šiame darbe — tiksli genų moduliacija lokalizuotose smegenų srityse — laikosi kelių potencialių kelių į žmogaus terapijas. Vienas kelias yra genų terapija su adeno‑susijusiais vektoriais, kitur — sezoninės ar laikinai aktyvios platformos, leidžiančios koreguoti ekspresiją tik tam tikrą laiką. Be to, galima plėtoti labai selektyvų farmacijos požiūrį: mažos molekulės arba biologiniai agentai, kurie blokuoja arba modulioja GluK4 turinčius receptorius (kainato tipo AMPA/Kainato receptorių šeima), galėtų pasiūlyti mažiau invazinius sprendimus. Visgi svarbu pabrėžti, kad kiekviena strategija turi savo privalumų ir trūkumų — nuo ilgaalaikio poveikio galimybių iki grėsmės imunologiniam atsakui ar nepageidaujamam persitvarkymui kitose grandinėse.
Praktinė perspektyva klinikoje taip pat apima saugos ir efektyvumo rodiklių identifikavimą, pavyzdžiui, veiksmingumo matavimus per pažinimo testus, socialinio funkcionalumo atstatymą, bei biomarkerių panaudojimą (neurovaizdavimo rodikliai, e‑biomarkerių profiliai), kad galėtume stebėti poveikį kontroliuotose klinikinių tyrimų sąlygose. Papildomos rekomendacijos apima darbinį modelių išplėtimą į didesnius graužikus ir primatus, ilgalaikes stebėjimo studijas, bei multimodalius tyrimus, sujungiančius molekulinius, elektrofiziologinius ir elgesio duomenis. Tokie žingsniai padidintų tyrimo atramos faktorių patikimumą ir prisidėtų prie etiškai pagrįstų ir technologiškai tvarių klinikinių bandymų dizaino.
Šiuo metu darbas suteikia aiškesnį mechanistinį vaizdą: mažas neuroninis disbalansas amigdaloje gali sukelti disproporcingą emocinį poveikį, o šio disbalanso koregavimas atkuria daugelį, bet ne visus simptomus. Šis atskyrimas yra esminis — jis nurodo, kurie simptomai gali būti tiesiogiai gydomi lokalizuotu genų modulavimu, o kurie gali reikalauti platesnių arba kombinuotų terapijų. Tolesni mechanistiniai tyrimai ir geresni translaciniai modeliai bus svarbūs tiek pagrindiniams moksliniams klausimams, tiek praktiniams sprendimams, susijusiems su nerimo sutrikimų gydymu ir neuropsychiatrine priežiūra ateityje.
Šaltinis: sciencealert

Palikite komentarą