7 Minutės
Mokslininkai iš Cincinnati Children’s Hospital Medical Center, bendradarbiaudami su Roche, sukūrė miniatiūrinę žmogaus kepenų platformą, gebančią modeliuoti imuninės kilmės vaistų reakcijas, kurios pasitaiko tik tam tikriems pacientams. Derindami pacientų ištirtas kamienines ląsteles su jų pačių imuninėmis ląstelėmis, tyrėjai laboratorijoje atkūrė retą, bet rimtą vaistų sukeltą kepenų pažeidimą — pažangą, kuri gali pakeisti vaistų saugumo vertinimo praktiką ir įvesti naujas priemones vaistų toksiškumo prognozavimui.
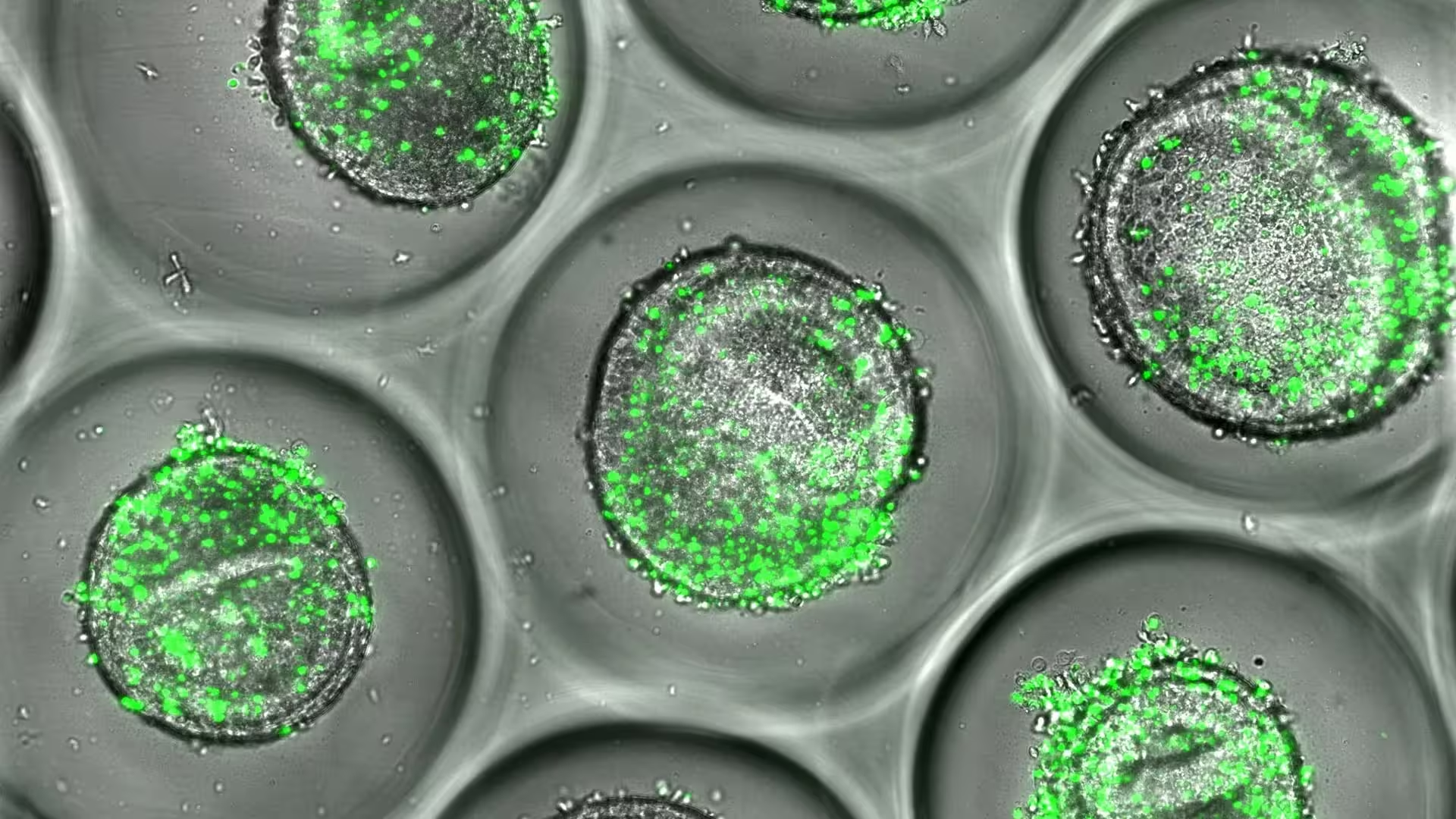
Pavyzdys: žmogaus kepenų organoidai, kartu kultivuoti su autologinėmis CD8 T ląstelėmis (žalia). Tokie audiniai gali būti naudojami vaistų kūrimo procese, siekiant prognozuoti kepenų toksiškumą ir sumažinti riziką pacientams, rodo naujas tyrimas, paskelbtas Cincinnati Children’s ekspertų.
Laboratorijoje užaugintos kepenys, išsaugančios genetinę atmintį
Vaistų sukeltas kepenų pažeidimas (DILI) yra viena iš pagrindinių ūminės kepenų nepakankamumo priežasčių ir dažna priežastis, dėl kurios vaistai išimami iš rinkos. Dauguma priešklininių tyrimų neprognozuoja retų, imunu grindžiamų DILI formų, vadinamų idiosinkraziniu DILI (iDILI), nes šios reakcijos priklauso nuo individualių genetinių ypatybių ir specifinių imuninės sistemos atsakų. Naujoji platforma užpildo šią spragą, sukurdama imuninę funkciją turintį, visiškai žmogaus pagrindu sukurtą kepenų modelį, įtraukiantį paciento genetiką ir imunitetą.
Sistema naudoja donoro išvestas indukuotas pluripotentines kamienines ląsteles (iPSC), kad sukurtų trimačius kepenų organoidus. Toks miniatiūrinių audinių tinklas tada yra derinamas su to paties donoro CD8+ T ląstelėmis — imuninėmis ląstelėmis, kurios neteisingai atpažinusios vaisto susijusius molekulinius signalus gali pulti hepatocitus. Gautas mikroarray išsaugo tiek genetinę, tiek imuninę individualumą, leidžiant tyrėjams stebėti, kaip konkrečios kombinacijos sukelia uždegimą, citokinų išskyrimą ir ląstelių pažeidimus.
Kaip organoidų mikroarray atkuria realaus pasaulio vaistų žalą
Kaip koncepcijos įrodymą, tyrėjai išbandė flucloksaciliną — antibiotiką, žinomą dėl kepenų pažeidimų tik tarp asmenų, turinčių HLA-B*57:01 geno variantą. Tradiciniai modeliai retai parodo šį efektą, tačiau organoidų ir autologinių CD8+ T ląstelių ko-kultūra sukūrė imuninės kilmės kepenų pažeidimo požymius: CD8+ T ląstelių aktyvaciją, padidėjusį uždegiminį signalavimą ir matomą hepatocitų pažeidimą. Toks glaudus atitikimas klinikiniams stebėjimams yra tai, kas daro šį metodą perspektyviu prognostinės toksikologijos įrankiu.
Vyriausiosios autoriai dr. Fadoua El Abdellaoui Soussi ir dr. Magdalena Kasendra paaiškina, kad pacientui specifinių imuniteto ląstelių integravimas buvo trūkstama dedamoji, reikalinga idiosinkrazinių reakcijų reprodukcijai. Kasendra, CuSTOM (Center for Stem Cell and Organoid Medicine) tyrimų ir plėtros direktorė Cincinnati Children’s, pabrėžia, kad tikslas yra užfiksuoti žmogiškąją biologiją skalėje, kuri yra pakartojama ir pritaikoma vaistų vystymo cikle — taip saugumo vertinimas gali būti atliekamas anksčiau ir patikimiau.
Nuo metodo iki vaisto: techniniai proveržiai
Platforma remiasi ankstesnėmis organoidų inovacijomis, naudojant be-matriksinę mikroarray technologiją ir laboratorijų patobulinimus, kurios turi patirties generuojant tvirtus kepenų organoidus iš iPSC. Toks derinys leidžia didesnį pralaidumą (throughput) nei tradicinės organoidų kultūros, tuo pačiu išlaikant esmines žmogiško imuninio atsako savybes. Kritisks reikšmės etapui buvo bendradarbiavimas su Roche, kuris atnešė translacinės toksikologijos kompetenciją bei resursus, spartinančius plėtrą ir validaciją.
Be vieno geno–vaisto sąveikos atkartojimo, mokslininkai automatizuoja testus ir plečia donorų bazę, siekdami aprėpti plačią genetinę įvairovę. Tikslas — sukurti atrankos sistemą, galinčią identifikuoti potencialų imuninės kilmės toksiškumą skirtingose populiacijose dar prieš pradedant klinikinius tyrimus. Toks gebėjimas sumažintų pacientų riziką vėlesniuose etapuose ir mažintų vėlyvos stadijos vaistų nesėkmių skaičių, taip pagerinant vaistų kūrimo ekonomiškumą ir pacientų saugumą.
Poveikis pacientams ir vaistų kūrėjams
Pacientams ši platforma atveria ateitį, kai saugumo tyrimai atsižvelgs į individualią genetinę riziką. Įsivaizduokite situaciją, kai vaisto kandidatas yra išbandytas prieš organoidų–imuniteto panelę, reprezentuojančią tūkstančius skirtingų genetinių profilių. Kūrėjai galėtų anksti identifikuoti pažeidžiamas pogrupes ir sukurti specialius klinikinius protokolus arba lydinčias diagnostines priemones (companion diagnostics), skirtas apsaugoti tuos pacientus.
Pramonės požiūriu, skalėjami žmogaus modeliai, atskleidžiantys imunitetu varomu toksiškumą, gali sumažinti atrankos nuostolius, pagreitinti sprendimų priėmimą ir galiausiai sumažinti išlaidas, susijusias su vėlyvosiomis nesėkmėmis. Darbas taip pat stiprina regeneracinę mediciną ir precizinę toksikologiją, sujungdamas kamieninių ląstelių mokslą su taikomu saugumo testavimu — integraciją, kuriai jau teikia paramą keli biotechnologijų ir instrumentų partneriai, įskaitant Molecular Devices ir Danaher.
Ekspertų įžvalgos
"Tai yra esminis žingsnis link tikrai prognostinės toksikologijos," teigia Dr. Elena Mora, klinikinė farmakologė Oksfordo universitete (komentaras pateiktas kaip kontekstas). "Modeliuodami, kaip paciento imuninė sistema sąveikauja su jų pačių kepenų audiniais, tyrėjai gali aptikti modelius, kuriuos praleidžia gyvūnų modeliai ar izoliuotos ląstelių kultūros. Tai nepakeis klinikinių tyrimų, bet padarys juos išmanesnius ir saugesnius." Ši ekspertų nuomonė pabrėžia svarbą integruoti žmogaus biologiją ankstyvose saugumo vertinimo stadijose.
Iššūkiai ir tolesnis kelias
Nors perspektyvos yra daug žadančios, iššūkių lieka. Organoidų gamybos mastelio didinimas išlaikant biologinį tikslumą nėra paprastas uždavinys, o užtikrinti, kad tyrimai būtų pakartojami skirtingose laboratorijose, reikalaus standartizacijos ir kokybės kontrolės procedūrų. Be to, imuninės kilmės reakcijos yra daugelio veiksnių rezultatas: aplinkos veiksniai, concomitantinė medikacija (kiti vartojami vaistai) ir lėtinės ligos gali moduliuoti riziką, kurią nulemia ne vien genetika ir CD8+ T ląstelių elgsena. Tyrėjų komanda pripažįsta šias ribas ir siekia automatizuoti procesus bei išplėsti donorų imtį, kad būtų užfiksuota daugiau šios sudėtingos problematikos niuansų.
Tyrimas, paskelbtas žurnale Advanced Science 2025 m. rugsėjo 26 d., išryškina Cincinnati Children’s CuSTOM Accelerator kaip lydere verčiant organoidų mokslą į praktinius įrankius. Pagal autorius, tai ankstyvas, bet reikšmingas žingsnis link vaistų saugumo personalizavimo — pokyčio, galinčio apsaugoti tą mažą žmonių pogrupį, kuris yra jautrus imuninės kilmės kepenų pažeidimams.
Kaip organoidų platformos bręsta, reguliuotojai, pramonė ir klinikiniai tyrėjai turi glaudžiai dirbti kartu, kad validuotų ir pritaikytų šias sistemas saugumo vertinimo grandinėje. Jei tai pavyks, naujos kartos priešklinikiniai testai bus labiau žmogaus biologiją atitinkantys, labiau prognostiniai ir geriau apsaugosi pacientus nuo retų, bet sunkių nepageidaujamų vaistų reakcijų. Taip pat svarbu, kad tokie modeliai būtų prieinami ir integruojami į reguliacinius gairių atnaujinimus, kad nauji testavimo standartai taptų tarptautiniu mastu priimtini ir taikomi klinikiniuose tyrimuose.
Techniniai niuansai, kuriais verta domėtis: iPSC kilmės kokybė, organoidų brandos laipsnis, antigenezės vystymasis in vitro, CD8+ T ląstelių kloninė įvairovė ir citokinų matavimų jautrumas — visi šie veiksniai lemia modelio našumą. Be to, duomenų analizė, įskaitant transkriptomiką, proteomiką ir funkcinius hepatocitų testus, suteikia daugiaplanius rodiklius, leidžiančius diferencijuoti tiesioginį vaisto toksiškumą nuo imuniteto mediatoriaus žalos. Kombinuotas omikos ir funkcinis požiūris stiprina gebėjimą identifikuoti biomedicinius žymenis (biomarkers), kurie gali būti perduodami tolesniems klinikiniams vertinimams ir companion diagnostic įrenginiams.
Praktinis diegimas reikalauja ne vien tik technologinio sukūrimo — tai taip pat reikalauja aiškių etinių ir duomenų apsaugos gairių, ypač kai dirbama su pacientų genetine informacija ir autologinėmis imuninėmis ląstelėmis. Siekiant išlaikyti pacientų konfidencialumą ir suderinti biologinius išteklius su klinikinėmis ir mokslinėmis reikmėmis, reikalingos griežtos atrankos, informuoto sutikimo ir duomenų valdymo procedūros. Tai svarbu tiek moksliniam patikimumui, tiek visuomenės pasitikėjimui tokiomis technologijomis.
Apibendrinant, ši organoidų ir imuniteto integracija suteikia naują įrankį precizinės toksikologijos arsenale: ji leidžia modeliuoti paciento-mastelio riziką, identifikuoti potencialius jautrius pogrupius ir padėti kurti saugesnius vaistus. Tolesnė automatizacija, plati genetinės įvairovės imtis ir tarptautinė standartizacija bus esminiai žingsniai, kad ši technologija būtų pragmatiškai pritaikyta vaistų kūrimo grandinėje ir reguliavimo procese.
Šaltinis: sciencedaily

Palikite komentarą