7 Minutės
Atraskimo santrauka: paslėptas receptorius, kontroliuojantis kaulų stiprumą
Leipzigo universiteto tyrėjai identifikavo anksčiau nepakankamai įvertintą receptorių — GPR133 — kuris veikia kaip molekulinis „kaulų jungiklis“, reguliuojantis skeleto stiprumą. Laboratoriniuose tyrimuose su pelėmis GPR133 aktyvavimas nauju mažu molekuliu AP503 padidino kaulų tankį ir atvertė pokyčius, panašius į osteoporozę. Šis darbas rodo naują biologinį tikslą terapijoms, galinčioms tiek išsaugoti, tiek atstatyti kaulus — svarbus poreikis senėjant populiacijoms.
Kodėl naujos osteoporozės gydymo priemonės yra skubiai reikalingos
Osteoporozė yra lėtinė liga, kuriai būdingas progresuojantis kaulų masės mažėjimas ir mikroarchitektūros degradacija, didinanti lūžių riziką. Vien Vokietijoje ja serga apie šeši milijonai žmonių, daugiausia moterų, ypač po menopauzės. Esamos gydymo priemonės — tokios kaip bisfosfonatai, denosumabas ar anaboliniai vaistai kaip teriparatidas ir romosozumabas — gali sumažinti lūžių riziką, tačiau turi ribojimų: nepageidaujamų poveikių, riboto vartojimo trukmės ir neišbaigto kaulų kokybės atkūrimo. Yra skubus poreikis saugesnėms ilgalaikėms strategijoms, kurios vienu metu užkirstų kelią kaulų nykimui ir atkurtų skeleto integralumą.
Siekiant rasti alternatyvų su geresniu saugumo ir veiksmingumo profiliu, mokslininkai tiria naujus molekulinius taikinius kaulų biologijoje. Vienas perspektyvus taikinys yra GPR133 — adhesinių G baltymų receptorių (adhesion GPCR) šeimos narys, kuris iki šiol buvo mažai tirtas kaulų pertvarkymo kontekste.
Mechanizmas: kaip GPR133 aktyvacija pertvarko kaulus
GPR133 priklauso membranos baltymų klasei, vadinamai adhesiniais G baltymų receptoriais. Šios molekulės aktyvuojamos mechaninių signalų ir ląstelių tarpusavio sąveikų bei perduoda signalus ląstelės viduje per G baltymus. Kaulų audinyje GPR133 aktyvacija paleidžia kaskadą, kuri padidina osteoblastų — naujus kaulus formuojančių ląstelių — aktyvumą, tuo pačiu slopindama osteoklastų — atsakingų už kaulų rezorbciją — veiklą. Nukreipdama pusiausvyrą į kaulų formavimą, GPR133 signalizacija stiprina kaulų struktūrą ir didina patvarumą.
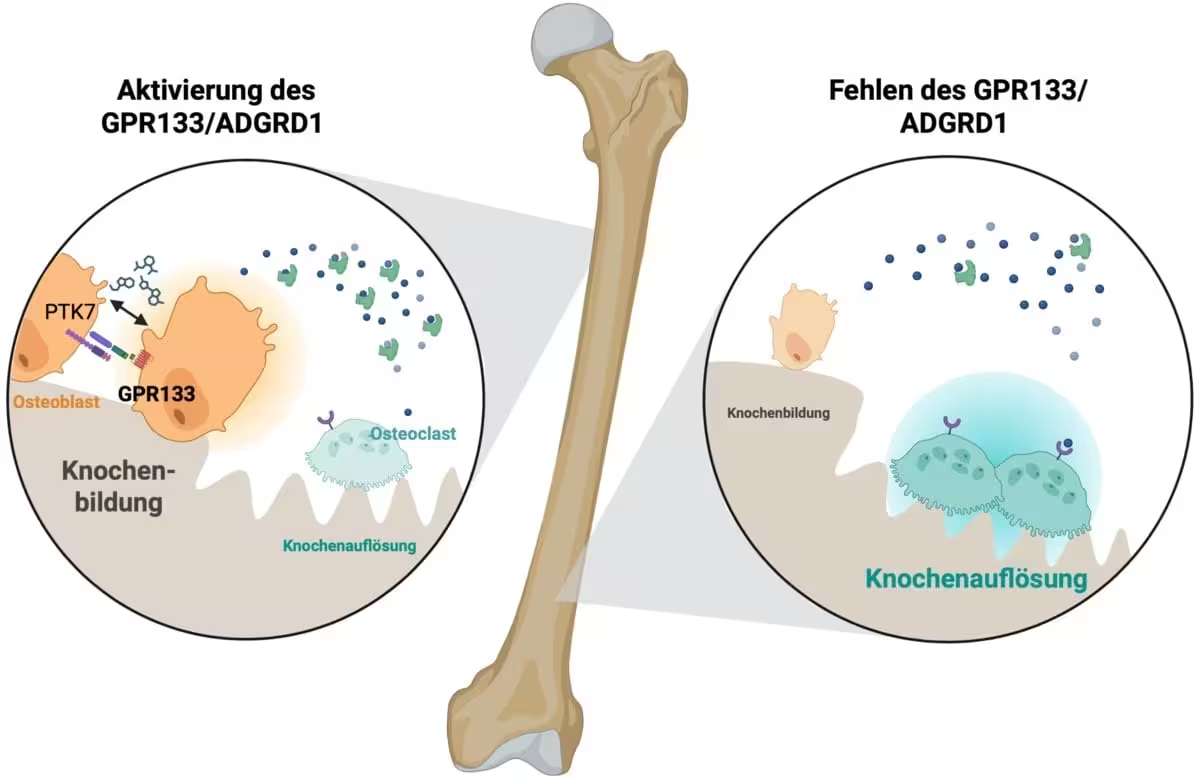
Aktyvinta GPR133 kaulų audinyje sukelia signalą, kuris skatina kaulus formuojančias ląsteles (osteoblastus) ir slopina kaulus ardžiančias ląsteles (osteoklastus). Šaltinis: Biorender, Ines Liebscher
Rudolf Schönheimer biochemijos institute atlikti laboratoriniai tyrimai parodė, kad GPR133 genetinis sutrikimas pelėms sukelia ankstyvą kaulų tankio sumažėjimą — fenotipą, atspindintį kai kurias žmogaus osteoporozės savybes. Priešingai, receptoriaus farmakologinis stimuliavimas naudojant AP503 — atrastą per kompiuterinę atranką — davė reikšmingą kaulų masės padidėjimą ir pagerino skeleto mechanines charakteristikas tiek sveikuose, tiek osteoporozę modeliuose esančiuose gyvūnuose.
Aktyvacijos būdai: mechaninis tempimas ir ląstelių sąveikos
GPR133 reaguoja į mechaninį tempimą ir į signalus, kilusius iš tiesioginių kaulų ląstelių sąveikų. Šis dvigubas jautrumas rodo, kad receptorius veikia kaip fiziologinis integratorius, apjungiantis tiek fizinį krūvį (treniruotės, svorio nešiojimas), tiek vietinę tarpląstelinę signalizaciją, verčiant šiuos signalus anaboliniais (kaulus formuojančiais) atsakymais.
Tyrimo išvados ir eksperimentiniai duomenys
Leipzigo tyrime mokslininkai naudojo molekulės genetiką, ląstelių biologiją ir in vivo farmakologiją. Pagrindiniai radiniai yra:
- Pelės su sumažinta GPR133 funkcija darėsi mažo kaulų tankio jauname amžiuje, kas rodo, kad receptorius reikalingas normaliam kaulų kaupimuisi ir palaikymui.
- AP503, mažoji molekulė, atrasta per didelio pralaidumo kompiuterinę atranką, selektyviai stimuliavo GPR133 ir atkartojosi jo natūralią anabolinę signalizaciją kauluose.
- Gydymas AP503 padidino kaulų mineralinį tankį, pagerino mikroarchitektūrą ir atvertė osteoporozei panašius pokyčius gydytose pelėse.
Šie preklinikiniai rezultatai palaiko idėją, kad taikant GPR133 galima tiek užkirsti kelią senatviniam kaulų nykimui, tiek aktyviai atstatyti jau prarastus kaulus. Vertėtų paminėti, kad ankstesni tos pačios grupės darbai parodė, jog AP503 taip pat stiprina skeleto raumenis, kas kelia galimybę koordinuotoms naudos formoms raumenų ir kaulų sveikatai — ypač pageidautina intervencijoms, skirtoms silpniems vyresnio amžiaus asmenims.
Klinikinės implikacijos ir vystymo iššūkiai
GPR133 ir AP503 identifikavimas atveria vertimą į kliniką, tačiau taip pat kelia įprastus iššūkius:
- Saugumas ir specifika: reikia išsamiai ištirti AP503 selektyvumą GPR133 atžvilgiu ir jo nepageidaujamą sąveiką su kitais taikiniais. Ilgalaikis GPCR signalizacijos moduliavimas reikalauja kruopščių toksikologinių tyrimų.
- Farmakokinetika ir tiekimas: cheminė optimizacija gali būti reikalinga užtikrinti gerą vartojamumą per burną, metabolinį stabilumą ir tinkamą dozę žmonėms.
- Veiksmingumas didesniuose žinduoliuose ir žmonėse: pelės modeliai yra informatyvūs, tačiau pilnai neperteikia žmogaus kaulų pertvarkos dinamikos. Reikės tyrimų su didesniais gyvūnais ir galiausiai etapinių klinikinių tyrimų, kad būtų įvertintas lūžių rizikos mažinimas ir funkciniai rezultatai.
Kadangi esami gydymo standartai jau mažina lūžių riziką, bet koks naujas gydymas turi parodyti arba pranašesnį veiksmingumą, geresnį saugumo profilį ilgalaikiam vartojimui, arba unikalią naudą, pavyzdžiui, vienu metu stiprinant raumenis. Galimybė tiek užkirsti kelią kaulų nykimui, tiek regeneruoti prarastus kaulus daro GPR133 ypač patraukliu farmacijos vystymo taikiniu.
Fonas ir tyrimų kontekstas: dešimtmetis GPCR studijų Leipzige
Leipzigo universitetas daugiau nei dešimtmetį investavo į adhesinių GPCR struktūrinį ir funkcionalų tyrimą per Bendradarbiavimo tyrimų centrą 1423 „GPCR aktyvacijos ir signalizacijos struktūrinė dinamika“. Šis ilgalaikis, koncentruotas darbas pavertė universitetą tarptautiniu adhesinių GPCR tyrimų centru ir leido taikyti daugiaspektinius metodus, kurie atskleidė GPR133 vaidmenį kaulų biologijoje.
"Jei šis receptorius yra sutrikdytas dėl genetinių pokyčių, pelės ankstyvame amžiuje parodo kaulų tankio praradimo požymius – panašius į osteoporozę žmonėms. Naudodami medžiagą AP503, kuri neseniai buvo identifikuota kompiuterine parinktimi kaip GPR133 stimulas, mums pavyko žymiai padidinti kaulų stiprumą tiek sveikose, tiek osteoporozės turinčiose pelėse," aiškina profesorė Ines Liebscher, pagrindinė tyrimo vadovė iš Rudolf Schönheimer biochemijos instituto Medicinos fakultete.
Ekspertų įžvalga
Dr. Martin Keller, hipotetinis translacinis farmakologas ir vyresnysis R&D patarėjas, turintis patirties raumenų ir kaulų vaistų kūrime, komentuoja: "Taikyti adhesiniams GPCR, tokiems kaip GPR133, yra protinga strategija, nes šie receptoriai stovi ant mechaninių stimulų ir ląstelių atsako sąsajos. Junginys, galintis saugiai imituoti fizinio krūvio sukeltą signalizaciją ir nukreipti pertvarkymą į kaulų formavimą, galėtų pakeisti ilgalaikį osteoporozės gydymą — ypač pacientams, kurie nepakelia dabartinių terapijų. Kelias nuo pelės iki rinkos yra ilgas, tačiau čia pranešta dviguba raumenų ir kaulų nauda ypatingai patraukli senatvinės priežiūros srityje."
Kitos žingsniai ir ateities perspektyvos
Leipzigo komanda vykdo keletą tęstinių projektų, siekdama išsamiau apibrėžti AP503 mechanizmą ir išbandyti receptoriaus vaidmenį kituose ligų modeliuose. Svarbūs tolesni žingsniai apima:
- Dozės-atsako ir lėtinio vartojimo tyrimai siekiant įvertinti išliekamąsias poveikio ir saugos charakteristikas.
- Struktūriniai tyrimai, kad būtų suprasta, kaip AP503 prisijungia ir aktyvina GPR133, palengvinant racionalią vaistų optimizaciją.
- Tyrimai didesniuose gyvūnų modeliuose, geriau prognozuojantys žmogaus farmakologiją.
- Ankstyvos stadijos klinikinis vystymas, jei preklinikinis saugumas ir veiksmingumas bus patvirtinti.
Jei šie keliai pasiseks, GPR133 agonistai galėtų tapti kitos kartos osteoporozės terapijomis, ypač skirtomis postmenopauzinėms moterims ir vyresnio amžiaus suaugusiesiems, kuriems padidėjusi trapumo lūžių rizika.
Išvada
GPR133 atradimas kaip kaulų stiprumo reguliatoriaus ir mažos molekulės aktyvatoriaus AP503 demonstravimas, gebantis padidinti kaulų tankį ir atstatyti osteoporozei panašius pokyčius pelėse, yra perspektyvus žingsnis kaulų biologijoje. Remiantis dešimtmečio adhesinių GPCR tyrimų Leipzigo universitete pasiekimais, šis darbas suteikia tiek naują terapinį taikinį, tiek koncepcinį pagrindą intervencijoms, apjungiančioms mechaninius ir ląstelinius signalus kaulų atstatymui ir išsaugojimui. Nors vertimas į žmogaus gydymą reikalauja išsamių tolimesnių tyrimų, galimybė vienu metu stiprinti kaulus ir raumenis kelia GPR133 moduliavimą kaip prioritetinę kryptį kovai su amžiumi susijusiu raumenų ir kaulų susilpnėjimu.
Mokslininkai rado „kaulų jungiklį“, galintį sustabdyti osteoporozę ir padėti išlaikyti kaulus stiprius su amžiumi. Šaltinis: Shutterstock
Aktyvinta GPR133 kaulų audinyje sukelia signalą, kuris skatina kaulus formuojančias ląsteles (osteoblastus) ir slopina kaulus ardžiančias ląsteles (osteoklastus). Šaltinis: Biorender, Ines Liebscher
Šaltinis: scitechdaily

Palikite komentarą