10 Minutės
Japonų mokslininkai sukūrė naujos kartos vitamino K molekules, kurios žymiai sustiprina smegenų gebėjimą kurti naujus neuronus. Chemiškai sujungę vitaminą K su retina rūgštimi, tyrėjai sukonstravo hibridines junginių rūšis, kurios neuronų diferenciaciją skatina daug veiksmingiau nei natūralus vitaminas K — tai atradimas, turintis potencialą kurti naujas terapijas Alzheimerio ligai ir kitoms neurodegeneracinėms ligoms gydyti.
Why neuronal regeneration matters now
Neurodegeneracinės ligos, tokios kaip Alzheimerio, Parkinsono ir Huntingtono liga, palaipsniui ardo neuronus — smegenų informacijos apdorojimo ląsteles. Kai neuronai žūsta arba praranda funkciją, pacientai patiria atminties sutrikimus, judėjimo sutrikimus ir nuolatinį pažinimo funkcijų silpimą. Dabartiniai vaistai daugiausia koreguoja simptomus; retai jos sugeba atkurti pažeistus neuronus ar juos regeneruoti. Ši spraga paskatino mokslininkus ieškoti regeneracinių strategijų: jei smegenis būtų galima paskatinti gaminti naujus neuronus iš progenitorinių ląstelių, pažeisti tinklai galėtų būti pataisyti arba stabilizuoti, o tai svarbu gydant neurodegeneracines ligas ir siekiant pagerinti pacientų gyvenimo kokybę.
Vitaminas K, riebaluose tirpus mikroelementas, geriausiai žinomas dėl savo vaidmens kraujo krešėjime ir kaulų metabolizme, pastaraisiais metais išryškėjo ir kaip netikėtas smegenų veiklos moduliatorius. In vitro tyrimai susiejo tam tikras vitamino K formas su neuronų išgyvenimu ir skatinimu pereiti į neuroninę diferenciaciją. Tačiau natūraliai pasitaikantys variantai, pavyzdžiui, menaquinonas-4 (MK-4), terapiniais tikslais dažnai pasižymi ribotu aktyvumu, todėl chemikai ir neurobiologai ėmė svarstyti, ar molekulinis perdizainavimas galėtų sustiprinti vitamino K neuroaktyvumą ir biologinę prieinamumą smegenyse.
Designing a more potent vitamin K
Shibaura Institute of Technology (Japonija) mokslininkai ėmėsi būtent tokio tikslo. Vyresnioji mokslo darbuotoja Yoshihisa Hirota ir profesorius Yoshitomo Suhara vadovaujama komanda sintezavo seriją hibridinių vitamino K analogų, chemiškai sujungdami vitamino K karkasus su retina rūgštimi — aktyviuoju vitamino A metabolitu, gerai žinomu dėl savo gebėjimo skatinti neuronų diferenciaciją. Tyrimo koncepcija derino dvi biologines funkcijas viename molekuliniame karkase, siekiant sukurti naują junginį su išplėstiniu neurogeniniu profiliu.
Iš viso komanda sukūrė 12 hibridinių homologų, kuriuose vitaminas K buvo sujungtas arba su retina rūgšties vienetu, arba su karboksilio rūgštine grupe, arba su metilesterio šonine grandine. Mokslinis tikslas buvo dvigubas: išsaugoti abiejų pirmtakų molekulių (vitamino K ir retina rūgšties) biologinius signalus ir patikrinti, ar sujungta molekulė sukelia stipresnį neuralinių progenitorių perėjimą į neuroninę kryptį nei atskiri komponentai. Tokia racionali cheminė dizaino strategija dažnai naudojama kuriant vaistus, kurie turi daugialypį tikslą — t. y. sujungti skirtingas veikimo mechanikas į vieną junginį.
Naudodami kultivuotas pelės neuralines progenitorines ląsteles, tyrėjai vertino dviejų branduolinių receptorių transkripcijos aktyvaciją: steroidų ir ksenobiotikų receptoriumi (SXR), kuriuo veikia vitaminas K, ir retina rūgšties receptoriumi (RAR), aktyvuojamu retina rūgšties. Svarbu tai, kad hibridiniai junginiai išlaikė aktyvumą abiejuose receptoriuose, o tai rodo, kad kiekviena funkcionali junginio dalis išliko biologiniu požiūriu aktyvi po cheminio sujungimo. Šis išlaikytas profilis yra svarbus — jis patvirtina, kad cheminis konjugavimas nepažeidė pagrindinių signalinių savybių.
Novel VK: a standout candidate
Tarp sintetintų junginių vienas hibridas — straipsnyje apibūdintas kaip Novel vitamin K analogue (Novel VK) — išsiskyrė ypatingu aktyvumu. Ši molekulė derino retina rūgšties konjugatą su metilesterio šonine grandine ir padidino neuronų diferenciaciją maždaug tris kartus, palyginti su natūraliu vitaminu K kontrolėje. Tyrėjai neuronų konversiją matavo stebėdami mikrotrubulius susijusį baltymą 2 (Map2), plačiai pripažintą brandžių neuronų žymenį.
Toks veiksmingumo padidėjimas nėra vien laboratorinis smalsumas: molekulė, kuri patikimai paskatina neuralinius progenitorius pereiti į neuroninę kryptį, turi potencialą būti vystyta kaip regeneracinis agentas, skirtas atstatyti smegenų ląsteles, prarastas dėl neurodegeneracijos. Be to, didesnis in vitro aktyvumas dažnai koreliuoja su mažesniais reikalingais dozės kiekiais in vivo, o tai yra privalumas kuriant saugesnius gydymo protokolus su mažesne toksinių šalutinių reiškinių rizika.
Novel VK aptikta ir kituose bioaktyvumo tyrimuose, kur ji rodė sutelktą poveikį diferenciacijos keliams, epigenetinėms modifikacijoms ir signalo transdukcijai, kas sudaro platesnį molekulės poveikio vaizdą. Tokie rezultatai skatina platesnę preklininių modelių analizę, apimančią tiek mechanistinius tyrimus, tiek funkcinius išgyvenimo ir integracijos į tinklus testus.
Peering into the mechanism: mGluR1 and epigenetic cues
Supratimas, kaip vitaminas K ir jo analogai inicijuoja neuronų diferenciaciją, buvo esminė komandos darbo dalis. Lyginant genų ekspresiją tarp MK-4 gydytų ląstelių ir ląstelių, paveiktų įvairių inhibitoriais, atsiskleidė netikėtas molekulinis partneris: metabotropiniai glutamato receptoriai (mGluR). Ypač mGluR1 išryškėjo kaip pagrindinis vitamino K genų reguliacinių ir epigenetinių efektų tarpininkas, susijusių su neuroninės brandos krypties pasirinkimu.
mGluR1 yra ląstelių paviršiaus receptorius, žinomas dėl savo vaidmens sinapsinėje signalizacijoje ir viduląsteliniuose kaskaduose. Ankstesni gyvūnų modeliai parodė, kad mGluR1 praradimas sutrikdo motorinį valdymą ir neuroninę komunikaciją — fenotipai, svarbūs neurodegeneracinėse ligose. Shibaura komanda pasitelkė skaičiaviminio struktūrinio modeliavimo ir molekulinio dokingo metodus, kad patikrintų, ar naujieji vitamino K analogai tiesiogiai sąveikauja su mGluR1. Simuliacijos patvirtino stiprų sąsajos ryšį tarp Novel VK ir mGluR1, kas atitinka išreikštus biologinius efektus ląstelių testuose.
Cellular uptake and conversion to active MK-4
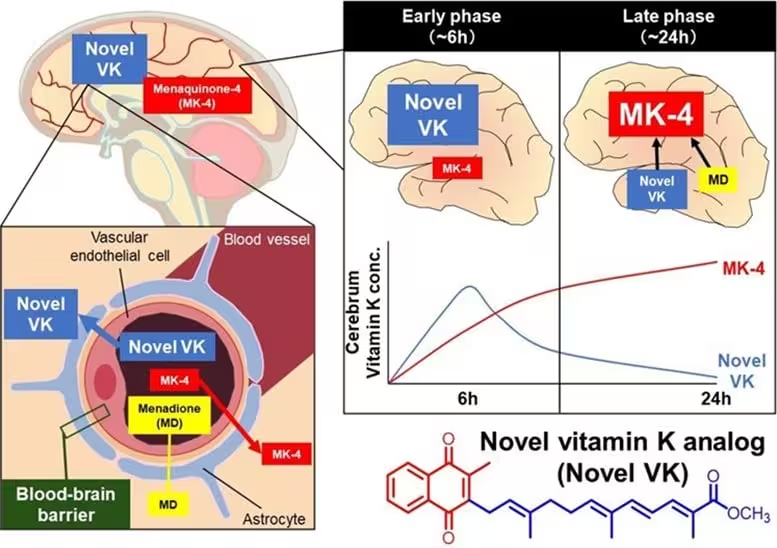
Kitas svarbus atradimas buvo efektyvumas, kuriuo Novel VK patenka į ląsteles ir yra paverčiama MK-4 — aktyvia intraceluline forma. Tiek ląstelių kultūroje, tiek in vivo pelėse intraceluliniai MK-4 kiekiai augo proporcingai Novel VK ekspozicijai. Palyginti su standartiniu vitaminu K, hibridas efektyviau konvertavosi į MK-4 ir pasiekė didesnes smegenų koncentracijas. Kritiškai svarbu, kad gyvūnų modeliuose buvo parodyta: Novel VK kerta hematoencefalinį barjerą ir pasižymi palankiu farmakokinetikos profiliu — esminė savybė bet kuriam centrinės nervų sistemos vaistui.
Tyrėjai patvirtino, kad Novel VK smegenyse sukėlė aukštesnius MK-4 lygius nei įprastos vitamino K formulės, kas sustiprina argumentą, jog cheminis pertvarkymas pagerina tiek molekulės aktyvumą, tiek biologinį prieinamumą. Tai turi tiesioginę reikšmę kuriant vaistus, nes smegenų koncentracijos ir ląstelinė konversija į aktyvų metabolitą dažnai nulemia terapinį poveikį.
Translational implications: toward vitamin K–based therapies
Šie rezultatai atskleidžia konkrečią trajektoriją nuo maistinės medžiagos biologijos prie galimų terapijų. Nustatę receptorius ir molekulinius kelius, įtrauktus į veikimą, tyrimas pateikia ne tik pirmąjį kandidatą (Novel VK), bet ir mechanistinį pagrindą tolesniam kūrimui. Jeigu tolimesni preklinikiniai ir klinikiniai tyrimai patvirtins saugumą ir efektyvumą, iš vitamino K išvesti vaistai galėtų tapti nauja regenracinės terapijos klase, kurios tikslas — sulėtinti arba atvirkščiai atstatyti neuronų netektį Alzheimerio ir kitose neurodegeneracinėse ligose.
Praktinių iššūkių vis dėlto netrūksta. Bet kuris kandidatas turi praeiti griežtą toksikologinį vertinimą, dozės optimizaciją ir ilgalaikio naudingumo demonstraciją gyvūnų modeliuose, kurie kuo geriau atspindi žmogaus ligos patologiją. Klinikinio tyrimo planavimo etape reikės atidžiai apgalvoti ligos fazę ir pacientų atranką: regeneracinės strategijos greičiausiai bus efektyviausios ankstyvose arba vidurio stadijose, kai neuraliniai progenitoriai ir išlikę smegenų tinklai dar gali reaguoti į diferenciacijos signalus.
Dr. Yoshihisa Hirota ir kolegos pabrėžia platesnę tokio požiūrio naudą: „Mūsų analogai parodo, kad nedideli cheminiai pakeitimai gali dramatiškai sustiprinti vitamino K neurogeninį potencialą. Tai atveria naujas galimybes terapijoms, kurios derina vitaminų saugumo profilį su tiksliniu molekuliniu aktyvumu,“ teigia komanda. Šis teiginys iliustruoja, kad maistinės medžiagos pagrindu sukurtos molekulės gali pasiūlyti ir saugumo, ir specifinio veikimo balansą, reikalingą tolimesniam vystymui į vaistus.
Shibaura Institute of Technology mokslininkai sukūrė ir sintezavo naujus vitamino K analogus, konjuguotus su retina rūgštimi, kurie pasižymi stipriu neuronų diferenciaciją skatinančiu aktyvumu. Jų išvados atskleidžia unikalius mechanizmus, paaiškinančius vitamino K ir jo analogų neuroprotekcinius efektus, ir sudaro prielaidas efektyvių gydymo priemonių kūrimui prieš neurodegeneracines ligas. Pateikimo šaltinis: Associate Professor Yoshihisa Hirota, Shibaura Institute of Technology, Japan
What this means for patients and the research pipeline
Pacientams ir jų prižiūrėtojams, susidurusiems su Alzheimerio liga ir panašiomis būklėmis, šis tyrimas suteikia daugiau vilties nei greito išgydymo pažadą. Artimiausio laikotarpio reikšmė greičiausiai bus susijusi su preklininiu tyrinėjimu: stipraus, į smegenis prasiskverbiantčio vitamino K analogo prieinamumas suteikia laboratorijoms naują įrankį neuronų regeneracijos, sinapsinio remonto ir ligai specifinių modelių tyrimui. Tokie įrankiai leidžia gilinti supratimą apie neurodegeneracijos mechanizmus ir testuoti kombinacines strategijas, pavyzdžiui, derinant Novel VK su fizine reabilitacija ar kognityvine terapija.
Plačiąja prasme efektyvi regeneracinė terapija galėtų sumažinti ilgalaikės priežiūros poreikį ir sveikatos priežiūros išlaidas, susijusias su progresuojančia demencija. Tačiau reikia pabrėžti: laboratoriniai pasiekimai ne visada tiesiogiai verčiasi klinikiniu pritaikymu; dažnai reikalingi metai ir nuoseklūs, griežti vertinimai, kad būtų užtikrintas saugumas ir poveikis žmonėms. Klinikinė vertė priklausys ne tik nuo molekulės veiksmingumo, bet ir nuo to, kaip gerai bus suprojektuoti tyrimai, pasirinkti tinkami biomarkeriai ir parinkti pacientų pogrupiai.

Viršelio vaizdas, kurį puošia straipsnis apie naujus vitamino K analogus, konjuguotus su retina rūgštimi, turinčius neuroprotekcinių savybių. Credit: ACS Chemical Neuroscience
Expert Insight
„Šis tyrimas elegantiškai sujungia mažųjų molekulių chemiją ir neuronų biologiją,“ pažymi Dr. Eleanor Park, fiktyvi neurofarmakologė ir mokslo komunikatorė. „Dvi išskiriančios dalys: racionalus dizainas, sujungiant vitamino K ir retina rūgšties motyvus, bei mechanistinis ryšys su mGluR1. Kartu tai sukuria nuoseklią grandinę nuo molekulės iki mechanizmo. Kitas kritinis žingsnis — patikrinti ilgalaikį poveikį ligai aktualiuose gyvūnų modeliuose ir užtikrinti saugumą terapinėmis dozėmis.“
Dr. Park priduria: „Retai pamatysi maistinės kilmės junginius, kurie ne tik praeina hematoencefalinį barjerą, bet ir tokia stipriai modifikuoja diferenciacijos kelius. Jei šios savybės patvirtins kitų tyrimų metu, rezultatai galėtų esmingai pakeisti mūsų požiūrį į neuroregeneraciją ir terapinį strategijų vystymą.“
Looking ahead: research priorities and future prospects
- Išplėsti preklinikinius bandymus Alzheimerio ir Parkinsono gyvūnų modeliuose, vertinant pažinimo ir motorinius rezultatus po Novel VK gydymo.
- Tirti ilgalaikį saugumą, galimus nepageidaujamus poveikius ir farmakodinamiką skirtingose amžiaus grupėse bei ligos stadijose.
- Patobulinti junginio cheminių savybių optimizaciją, siekiant dar geresnio smegenų pristatymo, metabolinio stabilumo ir receptorių selektyvumo.
- Planuoti ankstyvosios fazės klinikinius tyrimus, orientuotus į saugumą, neuronų regeneracijos biomarkerius ir funkcinę išeigą kruopščiai atrinktose pacientų grupėse.
Trumpai tariant, Shibaura Institute of Technology atliktas tyrimas pateikia įtikinamą koncepcijos patvirtinimą: chemiškai pagerinti vitamino K analogai gali būti stiprūs neuronų diferenciaciją skatinantys agentai, sąveikaujantys su reikšmingais nervų receptoriais, tokiais kaip mGluR1, praeinantys hematoencefalinį barjerą ir didinantys aktyvų MK-4 smegenyse. Tai sudaro esmines prielaidas perspektyviam terapiniam kandidatui, tačiau reikės metų intensyvių bandymų, kol tokie junginiai gali pasiekti klinikinius etapus ir galbūt vėliau — gydymo protokolus. Tuo tarpu technologinis ir mokslinis pažangumas suteikia papildomų galimybių integruoti tokius junginius į platesnį neurodegeneracijos tyrimų kontekstą, įskaitant derinimą su genų terapija, imunomoduliacija ar šiuolaikinėmis regeneracinės medicinos priemonėmis.
Šaltinis: scitechdaily


Palikite komentarą