4 Minutės
Keliasdešimt metų vartojamas kraujospūdį mažinantis vaistas hidralazinas atskleidė netikėtą molekulinį poveikį, kuris gali pakeisti nėštumo hipertenzijos gydymo ir net tam tikrų smegenų vėžio formų — ypač glioblastomos — terapijos perspektyvas. Tyrėjai teigia, kad šis atradimas atveria duris saugesnėms, tikslingesnėms gydymo strategijoms ir spartesnei vaistų kūrimo grandinei, perorientuojant gerai žinomą junginį į naujas indikacijas.
Kaip įsitvirtinęs vaistas atskleidė paslėptą mechanizmą
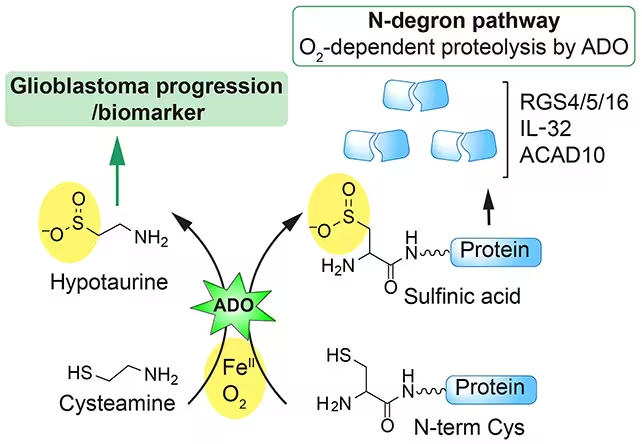
Mokslininkai, ieškoję atsakymo, kodėl hidralazinas padeda gydyti preeklampsiją — pavojingą kraujospūdžio padidėjimą nėštumo metu — aptiko anksčiau nežinomą molekulinį kelią, kuriam šis vaistas daro poveikį. Sistemȧs biocheminio žemėlapiavimo metodai, baltymų tarpusavio sąveikų analizė ir funkciniai eksperimentai leido identifikuoti konkrečias ląstelių signalizacijos grandines bei metabolinius procesus, kuriuos moduliuoja hidralazinas. Tokia mechanistinė informacija leidžia paaiškinti klinikinius vaisto privalumus ir pradėti kurti analogus, kurie išlaikytų efektyvumą, bet sumažintų šalutinį poveikį.
Kaip paaiškina chemikė Megan Matthews iš Pensilvanijos universiteto, molekulinio hidralazino veikimo supratimas suteikia gairę saugesniems ir selektyvesniems nėštumo hipertenzijos gydymo sprendimams kurti. Mechanizmo žinojimas taip pat teikia pranašumą vaistų kūrėjams: kadangi hidralazinas jau yra patvirtintas ir plačiai naudojamas, jo darinių arba patobulintų formulavimo kūrimas gali pasiekti pacientus žymiai greičiau nei visiškai nauji junginiai. Be to, esamas klinikinis saugumo profilis, farmakokinetiniai duomenys ir žinomi dozavimo intervalai suteikia tvirtą atspirties tašką pereinant nuo laboratorijos tyrimų prie klinikinių studijų.
Kodėl tai svarbu glioblastomai ir tikslinei terapijai
Už akušerijos ribų naujieji duomenys atkreipia dėmesį į specifines glioblastomos pažeidžiamumo sritis — agresyvios smegenų naviko formos, kuriai vis dar yra riboti gydymo variantai. Tyrimas rodo, kad hidralazinas trikdo tam tikrus ląstelių kelius, nuo kurių priklauso glioblastomos ląstelių išgyvenimas, prisitaikymas prie streso ir atsparumas terapijoms. Šiuos mechanizmus galima išnaudoti: jei pavyktų modifikuoti hidralaziną taip, kad jis selektyviai slopintų naviko apsaugos mechanizmus, tai galėtų tapti veiksmingu papildomu terapijos elementu kartu su radiacija, chemoterapija ar imuninės terapijos metodais.
Potencijos ir saugumo balansas
Vaistų pernaudojimas ar perorientavimas (drug repurposing) turi aiškų pranašumą — jau žinomą saugumo profilį ir klinikinį istoriją. Tačiau gydant smegenų vėžį ar nėštumo komplikacijas būtina subalansuoti: nukreipti poveikį į specifinius molekulinius taikinius, išsaugant sveikų audinių funkciją. Tai reiškia, kad reikės intensyvių medicininės chemijos pastangų formuojant hidralazino analogus su padidinta specifika, geresnėmis farmakokinetinėmis savybėmis (t. y. optimizuotas įsisavinimas, skaidymas, metabolizmas ir eliminacija) bei sumažintu toksiškumu. Be to, smegenų vėžio atveju būtina atsižvelgti į kraujagyslių smegenų barjerą (blood–brain barrier): modifikuoti junginiai turi pasiekti naviką reikiamu kiekiu, nekenkdami centrinei nervų sistemai.
Ką tai reiškia pacientams ir tyrėjams?
Tyrimų komanda savo rezultatus paskelbė žurnale Science Advances. Tolimesnės užduotys apima junginio selektyvumo tobulinimą, išsamius priešklinikinio lygmens bandymus, orientuotus į glioblastomos modelius, ir klinikines studijas, skirtas pagerinti preeklampsijos prognozę nėščioms moterims. Tokios studijos turėtų apimti ne tik veiksmingumo vertinimą, bet ir sudėtingesnį saugumo monitoringą, dozavimo schemų optimizavimą bei galimų vaistų sąveikų analizę, ypač kai gydant preeklampsiją tenka atsižvelgti į riziką vaisiui ir motinai.
Įsivaizduokime ateitį, kurioje senas kardiovaskulinis vaistas, perprojektuotas pagal šiuolaikines molekulines įžvalgas, padeda tiek besilaukiančioms moterims, tiek smegenų vėžio pacientams — tai būtų efektyvus kelias nuo laboratorinio atradimo iki klinikinės praktikos. Tokia strategija gali sutrumpinti laiką ir sumažinti kaštus, palyginti su visiškai naujų junginių kūrimu, o kartu išlaikant aukštą saugumo ir veiksmingumo lygį. Kaip pažymi M. Matthews, retai pasitaiko, kad klasikinis antihipertenzinis vaistas atvertų naujas neuro-onkologijos strategijas; tyrėjai viliasi, jog tai bus tik pradžia kryžminiams tarpdisciplininiams proveržiams, kurie tinkamai pritaikyti gali išsiversti į realius klinikinius sprendimus.
Šaltinis: sciencealert

Palikite komentarą