8 Minutės
Labai mažas, streso jautrus neuronų populiacijos segmentas, esantis giliai žievėje, gali koordinuoti kraujotaką ir elektrinę veiklą per visas smegenis. Nauji eksperimentai su pelėmis rodo, kad šios retos ląstelės — žinomos kaip I tipo nNOS neuronai — daro disproporcingai didelę įtaką miegui būdingiems smegenų ritmams, atliekų šalinimui iš smegenų audinio ir gali dalyvauti ankstyvuose neurodegeneracinių ligų etapuose. Ši hipotezė jungia kelis svarbius neuromokslų, neurovaskulinių tyrimų ir miego biologijos aspektus, todėl jų vaidmens supratimas gali turėti reikšmingų pasekmių prevencijos ir terapijos strategijoms, susijusioms su kognityvine būkle ir demencija.
Kaip kelios ląstelės veikia visą smegenų veiklą
I tipo nNOS neuronai yra retai pasitaikantis tipas ir daugiausia lokalizuoti giliuose žievės sluoksniuose; dėl savo mažo kiekio jie dažnai lieka nepastebėti tradiciniuose tyrimuose. Tačiau nauji duomenys rodo, kad šios ląstelės gali turėti centralizuotą reguliavimo funkciją, kuri nepaiso jų menko skaičiaus. Pensilvanijos Valstijos universiteto tyrėjai taikė tikslias, ląstelių specifines intervencijas, kad selektyviai pašalintų I tipo nNOS neuronus pelių modeliuose, o vėliau stebėjo smegenų kraujotaką (cerebralinę perfuziją), lėtus kraujagyslių pulso svyravimus, vadinamus vasomocija, ir bendrą neuroninį aktyvumą bei smegenų elektrinius ritmus. Tyrimo dizainas leido palyginti gyvūnus prieš ir po ląstelių pašalinimo ir analizavo tiek miego fazes, tiek budrumo periodus, siekiant nustatyti, kada pokyčiai yra ryškiausi.
Gauti rezultatai buvo akivaizdūs ir nuoseklūs. Gyvūnai, kuriems trūko I tipo nNOS neuronų, parodė sumažėjusią bendrą smegenų kraujotaką, silpnesnę vasomociją ir sumažintą neuronų išsikrovimų dažnį. Lėtosios delta bangos — smegenų ritmai, susiję su giliuoju miegu ir atminties konsolidacija — sumažėjo pagal amplitudę, o įprastas sinchronizacijos lygis tarp kairės ir dešinės pusrutulių pastebimai susilpnėjo. Toks vienu metu vykstantis kraujagyslių ir tinklo aktyvumo pokytis rodo, kad šios ląstelės gali veikti kaip centrinis koordinacinis elementas, suderindamos kraujo tiekimą su neuroniniu tinklu.
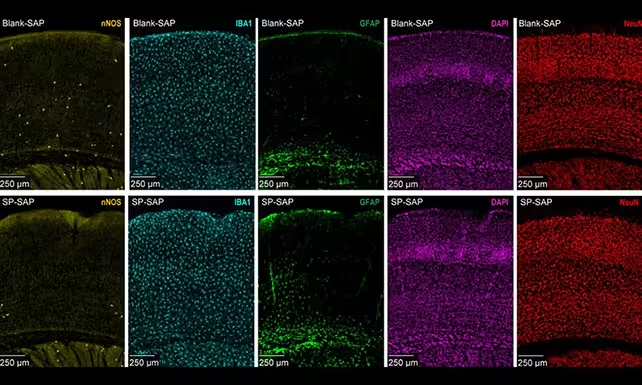
I tipo nNOS neuronai (geltonai pažymėti paveikslėlyje) yra gerokai retesni nei dauguma kitų neuronų tipų, ir jie buvo tiksliai pašalinti mokslininkų taikoma selektyvia abliacija.
Kodėl vasomocija ir lėtos bangos yra svarbios
Vasomocija apibūdina spontanišką, ritminį smegenų arterijų, venų ir kapiliarų išsiplėtimą bei susitraukimą kas kelias sekundes. Šios nuolatinės svyravimo fazės ne tik keičia hemodinamiką, bet ir skatina intersticinio skysčio ir cerebrospinalinio skysčio cirkuliaciją per smegenų audinį. Tokia fluidinė dinamika — dažnai minima kaip dalis glifatinės arba panašių atliekų šalinimo sistemų — padeda pernešti ir šalinti metabolinius produktus bei baltymus, kurie kitu atveju kauptųsi ir galėtų būti toksiški. Kai vasomocija susilpnėja, mažėja veiksminga atliekų išnešimo sparta, o tai gali prisidėti prie ląstelių streso ir baltymų, susijusių su Alzheimerio liga bei kitomis neurodegeneracinėmis patologijomis, sankaupų.
Pensilvanijos tyrimų komanda pastebėjo, kad kraujotakos ir neuroninio aktyvumo sumažėjimas buvo ypač ryškus miego metu — laikotarpiu, kai lėtos delta bangos paprastai dominuoja ir kai smegenų atliekų valymo mechanizmai yra aktyviausi. Šis ryšys kelia svarbią galimybę: jeigu I tipo nNOS neuronai yra pažeidžiami ar nyksta — dėl lėtinio streso, uždegimo ar natūralaus senėjimo — tai gali iškreipti miego architektūrą, sumažinti lėtų bangų aktyvumą ir tuo pačiu susilpninti smegenų „naktinį valymą“. Laikui bėgant, tokie pokyčiai gali prisidėti prie kognityvinio nuosmukio ir padidinti riziką neurodegeneracinėms ligoms.
Eksperimentiniai duomenys ir platesnės pasekmės
Naudodami ląstelių specifišką abliaciją pelių modeliuose, tyrėjai sugebėjo išskirti I tipo nNOS neuronų vaidmenį be plataus lokalinių audinių pažeidimo. Toks selektyvumas yra svarbus, nes leidžia susieti konkretaus neuronų potipio praradimą su tarpdisciplininiais rezultatais: sumažėjusia spontaninės vasomocijos amplitudė, susilpnėjusia lėtų bangų veikla ir bendros smegenų hemodinamikos pokyčiais. Šie susieti pakeitimai kraujagyslių ir neuroniniuose procesuose rodo, kad paveiktos ląstelės gali veikti kaip mazgas — hub — kuris laiko ritmą ir sinchronizaciją tarp kraujotakos reguliavimo bei neuroninių tinklų veiklos.
Biomedicinos inžinierius Patrick Drew, kurio laboratorija anksčiau žemėlapiavo nNOS susijusios kraujotakos reguliacijos mechanizmus, apibūdina spontanišką svyravimą kaip smegenų priemonę perkelti skystį ritmiškai plečiant ir siaurinant kraujagysles kas kelias sekundes. Jo ir kolegų interpretacija yra tokia: neuronų, kurie laiko ir koreguoja šiuos svyravimus, netekimas gali sukelti funkcinę kaskadą — nuo miego sutrikimų iki sumažėjusio atliekų pašalinimo — ir galiausiai paveikti ilgalaikę smegenų sveikatą bei atsparumą neurodegeneraciniams procesams. Ši koncepcija susieja vietinę neurovaskulinę kontrolę su globaliomis tinklo funkcijomis ir pabrėžia, kad net labai mažos neuronų populiacijos gali turėti didelį sisteminį poveikį.
Nuo pelių prie žmonių: kas atrodo tikėtina?
Reikėtų pažymėti, kad surinkti duomenys gaunami iš pelių modelių, o tiesioginis perkėlimas į žmogaus smegenis reikalauja papildomų tyrimų. Tačiau daugelis fundamentalių vaskulinių ir neuroninių procesų yra išsaugoti tarp žinduolių, todėl idėja, kad maža, streso ir senėjimo atžvilgiu pažeidžiama neuronų populiacija gali paveikti viso smegenų organo dinamiką, yra įtikinama. Jei panašios ląstelės egzistuoja ir žmonių smegenyse, jų praradimas dėl lėtinio streso, uždegimo, metabolinių sutrikimų arba paties senėjimo gali būti anksčiau nepakankamai įvertintas neurodegeneracijos veiksnys.
Sumažinta cerebralinė kraujotaka jau pripažįstama kaip vienas iš veiksnių, prisidedančių prie sutrikusios pažinimo funkcijos ir demencijos rizikos. Nauji duomenys suteikia papildomą sluoksnį: jie identifikuoja specifinį ląstelių tipą, kuris susieja vaskulinį tonusą, lėto miego bangų aktivumą ir tarppusinę (interhemisferinę) sinchronizaciją — visi šie komponentai yra svarbūs smegenų funkcinės sveikatos palaikymui. Ši interpretacija pabrėžia kompleksišką smegenų hemodinamikos ir tinklo aktyvumo priklausomybę ir rodo, kad klinikiniai parametrai, kaip periferinė kraujotaka ar miego kokybė, gali turėti gilias priežastines sąsajas su mikroskopinėmis neuroninėmis populiacijomis.
Ką tyrėjai planuoja tirti toliau
Ateities eksperimentai turės patvirtinti, ar žmogaus smegenyse egzistuoja ekvivalentinė I tipo nNOS neuronų populiacija ir ar ji atlieka panašią reguliacinę funkciją. Mokslininkai taip pat gilinsis į mechanizmus, kuriais stresas, uždegimas arba senėjimas selektyviai pažeidžia šias ląsteles, ir ar toks praradimas iš tikrųjų pirmauja prieš matomus pažinimo sutrikimus. Bus analizuojami molekuliniai žymenys, sinaptiniai ryšiai su kitais neuronų tipais, vaskuliniai prijungimai ir genetiniai bei epigenetiniai profiliai, kurie gali leisti identifikuoti pažeidžiamumo faktorius. Tokie tyrimai atvers kelią terapiniams bandymams — nuo neuroprotekcinių priemonių, mažinančių streso poveikį, iki tikslingų metodų, atkuriant arba išsaugant specifinius neuronų populiacijos funkcionalumus.
Jeigu ryšys tarp I tipo nNOS neuronų ir smegenų atliekų šalinimo, miego kokybės bei hemodinamikos bus patvirtintas ir žmonėms, apsauga arba atkūrimas šios neuronų kohortos galėtų tapti nauju taikiniu siekiant pagerinti miego kokybę, skatinti efektyvų smegenų „valymą“ per miegą ir sulėtinti kai kurių neurodegeneracinių procesų progresiją. Tokia strategija galėtų apimti tiek gyvenimo būdo intervencijas (pvz., streso valdymą, miego higieną, fizinį aktyvumą), tiek medikamentines priemones arba neuromoduliacines technologijas, skirtas palaikyti vasomocijos ir lėtų bangų veiklos sinchroniją.
Eksperto įžvalga
Dr. Claire Mendoza, neurovaskuliarinių tyrimų specialistė, nebuvo susijusi su šiuo tyrimu, tačiau komentuoja: "Mintis, kad reta neuronų rūšis gali koordinuoti vaskulinius ritmus visose smegenyse, yra įdomi ir potencialiai paradigmos keičianti. Tai peržiūri mūsų supratimą apie kraujotakos reguliaciją — ne vien kaip lokalią reakciją į neuroninį aktyvumą, bet kaip tinklų procesą, kuris palaiko miegą ir atliekų pašalinimą. Tirti šių neuronų atsparumą ir pažeidžiamumą gali atverti naujas prevencines strategijas demencijai."
Taip pat svarbu suprasti, kaip stresas veikia šiuos neuronus, nes lėtinis stresas yra plačiai paplitęs šiuolaikiniame gyvenime. Jei stresas selektyviai silpnina ląsteles, kurios reguliuoja cerebrinę kraujotaką ir vasomociją, tuomet streso mažinimas bei intervencijos, saugančios kraujagyslių sveikatą, gali būti reikšmingas kelias išsaugoti smegenų funkciją ir sumažinti kognityvinio nuosmukio riziką su amžiumi. Integruojant elgesio, farmacologines ir galbūt neuromoduliacines priemones, bus galima kurti holistines strategijas, skirtas išsaugoti tiek smegenų hemodinamiką, tiek miego kokybę ir taip prisidėti prie ilgalaikės smegenų sveikatos palaikymo.
Šaltinis: sciencealert

Palikite komentarą