5 Minutės
Pilki plaukai gali nešti paslėptą žinutę iš jūsų biologijos: kai kuriais atvejais pigmento netekimas labiau primena apsauginę reakciją nei kosmetinę ypatybę. Japonijos mokslininkų komanda, naudodama pelių modelius, parodė, kad melanocitų kamieninės ląstelės — ląstelės, suteikiančios plaukams spalvą — gali reaguoti į DNR pažeidimus būdais, kurie arba apsaugo nuo, arba skatina odos vėžio atsiradimą.
Kaip DNR pažeidimai, pigmentas ir vėžys yra susiję
Mūsų oda ir plaukai yra pirmosios linijos audiniai, nuolat veikiami genotoksinių aplinkos veiksnių: ultravioletinės šviesos, cheminių kancerogenų ir spinduliuotės, kurie sukelia DNR pažeidimus. Tokie poveikiai gali pagreitinti senėjimą ir padidinti vėžio riziką, tačiau kaip jie atsispindi matomuose požymiuose, tokiuose kaip plaukų žilimas, iki šiol buvo neaišku.
Naujas tyrimas susitelkia į melanomą — pavojingą odos vėžio formą, kilusią iš melanocitų, pigmentą gaminančių ląstelių, kurios vystosi iš melanocitų kamieninių ląstelių (McSCs) plaukų folikuluose. Profilizuodami genų raišką ir stebėdami ląstelių likimus pelėse, mokslininkai atseko skirtingas McSCs reakcijas į įvairius DNR pažeidimus.
Seno-diferenciacija: pigmentą keičiant saugumu
Kai McSCs patirdavo dvigubos grandinės DNR pertraukas — sunkią žalą, kai abi DNR grandinės yra pertraukos — jos linkdavo pereiti į negrįžtamą diferenciaciją ir išnykti. Procesas, autorių apibūdintas kaip senescence-coupled differentiation arba „seno‑diferenciacija“, priklauso nuo p53-p21 kelio aktyvacijos, kuris yra pagrindinis ląstelių ciklo sustabdymo ir pažeidimų reakcijų reguliatorius. Matomas rezultatas: plaukai praranda pigmentą ir pabąla.
Funkciniu požiūriu tai elegantiška biologija. Leidžiant pažeistoms kamieninėms ląstelėms išeiti iš savaime atsinaujinančio baseino, sumažėja ilgalaikė rizika, kad viena iš jų sukaups papildomų mutacijų ir taps naviko šaltiniu. Kitaip tariant, šiek tiek žilumo gali reikšti, kad organizmas teikia pirmenybę bendram saugumui prieš kosmetinę išvaizdą.
Kai pažeidimas neišprovokuoja saugiklio
Ne visi genotoksinai sukelia apsauginį kelią. Kai tyrėjai pelių odą veikė kancerogenais, tokiais kaip ultravioletinė B (UVB) spinduliuotė ir 7,12-dimetilbenz(a)antracenas (DMBA) — cheminė medžiaga, dažnai naudojama navikams sukelti laboratoriniuose modeliuose — pažeistos McSCs elgėsi kitaip. Vietoj to, kad išeitų per seno‑diferenciaciją, jos toliau atsinaujino ir kloniškai daugėjo.
Toks tęstinis atsinaujinimas buvo varomas vietinių kamieninių ląstelių nišos signalų, ypač kamieninių ląstelių faktoriaus (SCF), citokino, nukreipiančio melanocitus ir slopinančio seno‑diferenciaciją. Kancerogenų paveiktoje aplinkoje SCF ir susiję keliai, įskaitant KIT signalizaciją ir pakeistą arachidono rūgšties metabolizmą, leido pažeistoms McSCs išlikti ir daugintis — molekulinis kelias, galintis skatinti melanomos susidarymą, o ne pigmento praradimą.
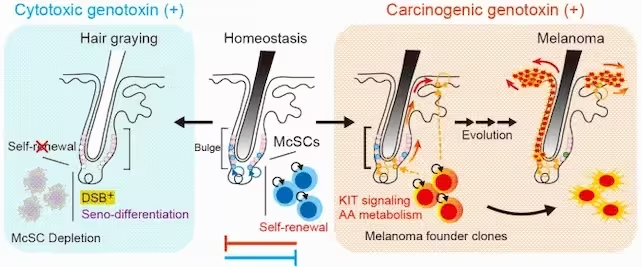
Esant citotoksiniams genotoksinams, pavyzdžiui rentgeno spindulių apšvitai, McSCs atsinaujinimas sutrinka, dėl to jos išeikvojamos ir plaukai žyla. Homeostazėje McSCs palaiko atsinaujinimą ir pigmentų pusiausvyrą. Tačiau kancerogeniniai genotoksinai skatina KIT signalizaciją ir keičia arachidono rūgšties metabolizmą, taip sukeldami melanomą. (University of Tokyo)
Kodėl tai svarbu odos senėjimui ir melanomai
Tyrimas persvarsto plaukų žilimą ir melanomą kaip alternatyvias pasekmes to, kaip kamieninės ląstelės susidoroja su stresu. Jei kamieninių ląstelių populiacija pasirenka išsekimą per seno‑diferenciaciją, audinys praranda pigmentą, bet gali įgyti apsaugą nuo naviko pradžios. Jei mikroaplinka invece teikia išgyvenimo signalus, pažeistos kamieninės ląstelės gali plėstis ir padidinti vėžio riziką.
Svarbu pabrėžti, kad mokslininkai yra atsargūs: patys pilki plaukai nėra įrodyta apsauga nuo vėžio žmonėms. Darbas naudoja pelių modelius, kad atskleistų molekulinius tinklus ir tikėtinas mechanikas. Tų pačių dinamikų patvirtinimas žmogaus odoje reikalauja papildomų tyrimų, kurie ištirtų žmogaus McSCs elgseną, aplinkos poveikius ir nišos signalizaciją, susijusią tiek su pigmento praradimu, tiek su melanomos dažniu.
Eksperimentiniai duomenys ir molekuliniai dalyviai
Komanda sujungė genų raiškos profilizavimą, tikslingus DNR žalojimo metodus ir ląstelių linijų sekimą pelėse. Jie išskyrė dvi plačias žalos aplinkybes: citotoksinius genotoksinus, tokius kaip jonizuojanti spinduliuotė, kurie skatina p53-p21 aktyvaciją ir seno‑diferenciaciją; ir kancerogeninius poveikius, tokius kaip UVB ir DMBA, kurie įtraukia augimą palaikančius nišos veiksnius ir blokuoja diferenciacijos saugiklį.
Pagrindinės išryškintos molekulės apima p53 ir p21 (pažeidimų jutikliai ir ląstelių ciklo reguliatoriai), SCF (kamieninių ląstelių faktorius) ir KIT signalizaciją (iš nišos kilę išgyvenimo signalai), be to — pokyčius arachidono rūgšties metabolizme, kurie, atrodo, siejasi su uždegimu, skatinančiu naviką. Šie keliai sieja molekulinę reakciją su matomais rezultatais: plaukų žilimu prieš melanomos vystymąsi.
Pasekmės prevencijai ir terapijai
Supratimas apie signalus, kurie nulemia, ar McSCs linksta prie išsekimo ar plėtros, atveria galimas intervencijas. Ar SCF/KIT signalizacijos arba uždegiminės aplinkos moduliavimas galėtų paskatinti pažeistas kamienines ląsteles saugiai pašalinti? Ar nišos aktyvumą atitinkantys biomarkeriai galėtų padėti identifikuoti odą, kuriai gresia didesnė melanomos rizika dar prieš atsirandant navikams?
Transliacinės perspektyvos šiuo metu yra spekuliatyvios, bet konceptualinis pažanga aiški: audinių senėjimas ir vėžys nėra nepriklausomi reiškiniai; jie gali būti skirtingos pasekmės to, kaip kamieninės ląstelės reaguoja į genotoksinį stresą.
Eksperto įžvalga
Dr. Maya Reynolds, dermatologė ir kamieninių ląstelių tyrėja (fiktyvi), apibendrina tyrimo praktinį aspektą: „Šis darbas sieja matomą senėjimą — pavyzdžiui žilimą — su giliais molekuliniais sprendimo taškais kamieninėse ląstelėse. Jei išmoksime perskaityti šiuos sprendimus žmogaus odoje, galime įgyti naujus ankstyvo įspėjimo žymenis melanomos rizikai nustatyti ir naujas prevencines strategijas, veikiančias kamieninės ląstelės nišą, o ne patį naviką.“
Tolimesni tyrimai turės patvirtinti šiuos kelius žmogaus audiniuose, nustatyti, kaip gyvenimo trukmės ekspozicijos veikia McSCs likimą, ir ištirti, ar nišos signalų manipuliavimas gali sumažinti melanomos paplitimą nekenkiant normaliam audinių palaikymui.
Šaltinis: sciencealert


Palikite komentarą