7 Minutės
Peržiūrint Alzheimerio ligą: imuninė klaida smegenyse
Alzheimerio liga vis dažniau suvokiama ne vien tik kaip baltyminė patologija (proteinopatija), bet ir kaip sutrikimas, kuriam daug įtakos turi smegenų imuninė reakcija. Šiuo nauju požiūriu smegenų imuninės ląstelės, ypač mikroglija, gali klaidingai atpažinti neuronų komponentus kaip svetimkūnius ir paleisti ilgalaikę gynybinę reakciją. Tokia chroniška neuroinflamacija laipsniškai silpnina neuronų funkcijas, trikdo sinaptinį perdavimą ir galiausiai lemia kognityvinį nuosmukį bei atminties praradimą — pagrindinius demencijos požymius.
Šio požiūrio centre yra beta-amiloido (Aβ) dvilypumas. Ilgą laiką beta-amiloidas laikytas pagrindine amiloidinių plokštelių sudedamąja dalimi, tačiau vis daugiau duomenų rodo, kad Aβ turi ir antimikrobinį arba imuninę paramą teikiančią funkciją: jis gali neutralizuoti mikrobus ir stiprinti įgimtą imuninę gynybą. Deja, kai beta-amiloidas kaupiasi, formuoja oligomerus arba praranda reguliaciją, jis gali sustiprinti imuninį aktyvumą ir palaikyti savitikslę ataką prieš smegenų audinį. Toks autoimuninio tipo procesas padeda paaiškinti, kodėl sisteminio poveikio imunosupresantai, pavyzdžiui, kortikosteroidai, kurie naudojami reumatoidiniam artritui gydyti, Alzheimerio ligai duoda ribotą naudą — centrinės nervų sistemos imuninė aplinka yra specifinė, o jai reguliuoti reikalingi specialūs agentai.
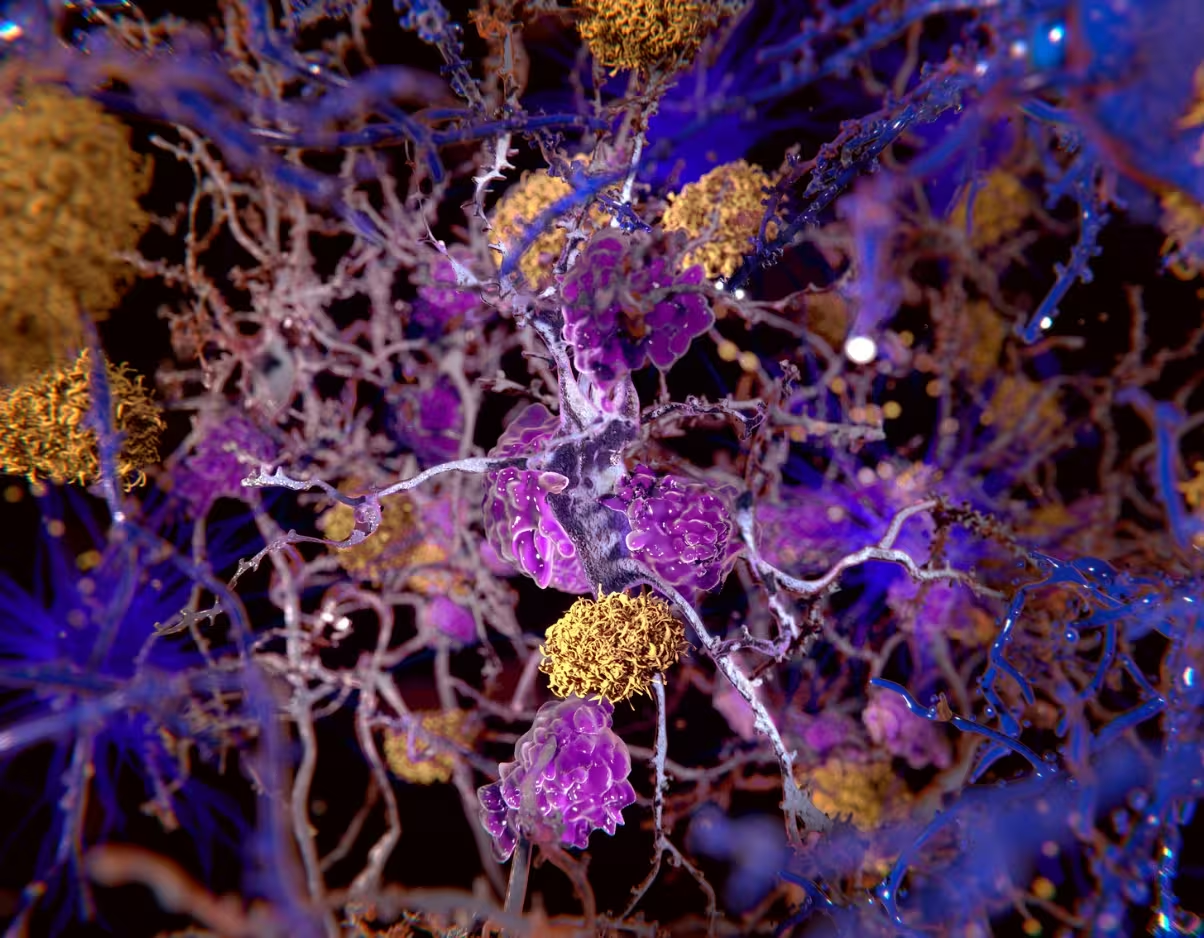
Beta-amiloido plokštelių (geltonai) iliustracija tarp neuronų.
Mokslinis fonas ir alternatyvios hipotezės
Šiuolaikiniai tyrimai plečiasi už vienintelės Alzheimerio ligos priežasties paaiškinimo ribų. Egzistuoja kelios konkuruojančios ir papildančios teorijos, kurios gali sąveikauti tarpusavyje ir bendromis mechanikomis lemti neurodegeneraciją. Svarbu paminėti, kad Alzheimerio ligos etiologija tikriausiai yra daugialypė — genetiniai polinkiai, senėjimas, metaboliniai sutrikimai ir aplinkos veiksniai gali susijungti į sudėtingą patogenezės tinklą.
- Mitochondrijų disfunkcija: Mitochondrijos užtikrina energijos gamybą (ATP) ir reguliuoja oksidacinį stresą. Jei neuronalų mitochondrijų veikla sumažėja arba generuojamas perteklinis mitochondrijinis reaktyvus deguonies rūšys (ROS), sutrinka sinaptinis perdavimas, degradacija baltymų apykaitoje ir atsiranda energijos deficitas, kuris ypač paveikia sinaptines funkcijas ir atmintį. Mitochondrijų pažeidimai taip pat gali skatinti tau baltymo fosforilinimą ir skatinti amiloido agregaciją.
- Chroninės infekcijos hipotezė: Kai kurie mokslininkai teigia, kad pasikartojančios arba lėtinės infekcijos — įskaitant burnos bakterijas (pvz., Porphyromonas gingivalis) ar virusus (pvz., Herpes simplex virus 1) — gali patekti į smegenis arba nuolat aktyvinti imuninį atsaką ir sukaupti uždegimą, kuris su laiku pereina į neurodegeneraciją. Tam pritinka duomenys apie mikroorganizmų grotelius smegenų audiniuose ir galbūt Aβ kaip antimikrobinį peptidą, iškart reaguojantį į mikrobinę grėsmę.
- Metalo disbalansas: Svarbūs metalai — cinkas, varis, geležis — reguliuoja daugelį neuroninių procesų, bet jų netinkama homeostazė gali skatinėti toksinių baltymų agregaciją ir oksidacinę žalą. Pavyzdžiui, geležies perteklius gali skatinti Fenton reakciją ir generuoti laisvuosius radikalus; vario ir cinko sąveika su Aβ keičia jo agregacijos kinetiką.
Šios hipotezės nėra vienas kitam priešingos — jos gali būti tarpusavyje susijusios. Pavyzdžiui, infekcija gali paskatinti beta-amiloido gamybą kaip apsauginį atsaką, o vėliau pernešti procesą į destruktyvų uždegimą pažeidžiamuose asmenyse. Lygiai taip, mitochondrijų disfunkcija gali padidinti pažeidžiamumą infekcijai ar oksidaciniam stresui, o metalų disbalansas gali pagreitinti baltymų agregaciją.
Gydymo ir tyrimų pasekmės
Jeigu Alzheimerio liga iš dalies yra imuninės atsakomosios reakcijos išsišokimas centrinėje nervų sistemoje, gydymo strategijos turi būti nukreiptos į smegenų specifinius imuninio reguliavimo kelius. Tai reiškia, kad terapijos, veikiančios sisteminę imuninę sistemą, nebūtinai duos norimą efektą, jeigu jos nepatenka į smegenų aplinką arba nepakeičia mikroglijos bei lokalių citokinų tinklų elgsenos.
Tarp perspektyvių krypčių minimos šios:
- Microglijos moduliacija: Mikroglija yra pagrindinė imunė barjera smegenyse. Nustatant jos fenotipų pokyčius (pro-inflamatoriniai M1 tipo arba rezolucijos M2 tipo analogai), galima nukreipti vaistus, kurie slopina chronišką pro-inflamatorinį aktyvumą arba skatina regeneracinę funkciją. Tyrimai su CSF1R inhibitoriais, taip pat su TREM2 moduliatoriais, siekia pakeisti mikroglijos atsaką ir pagerinti fagocitozę be pernelyg didelio uždegimo.
- Blogo uždegimo slopinimas smegenyse: Reikia antiuždegiminių agentų, kurie praeina kraujo‑smegenų barjerą (BBB) arba specifiškai veikia centrinėje nervų sistemoje. Inhibitoriai, nukreipti prieš NLRP3 inflammasomos kaskadą, citokinus (pvz., IL‑1β) ar komplemento sistemą, yra aktyviai tiriami kaip galimi terapiniai taikiniai, siekiant nutraukti uždegiminį ciklą.
- Beta-amiloido dinamikos atstatymas: Vietoj visiško Aβ pašalinimo verta siekti homeostazės atkūrimo — slopinti patogenezinius oligomerus ir mažinti plokštelių formavimą be Aβ apsauginės antimikrobinės funkcijos praradimo. Monokloniniai antikūnai, tokie kaip tie, kurie nukreipti prieš specifines Aβ formos struktūras (oligomerai prieš fibriles), bei mažesnės molekulės, modifikuojančios Aβ apykaitą, yra svarstomi gydymo arsenale.
- Biomarkeriai ir tikslinė medicinos praktika: Tikslinė terapija reikalauja patikimų biomarkerių, skirtų atskirti antimikrobinį atsaką nuo patologiško autoimuninio proceso. CSF ir plazmos rodikliai (Aβ42/40 santykis, p‑tau, total tau, neurofilamento lengvasis baltymas — NfL), taip pat PET vaizdinimo žymenys amiloidui ir tau, yra svarbūs atrankai ir gydymo rezultatų vertinimui.
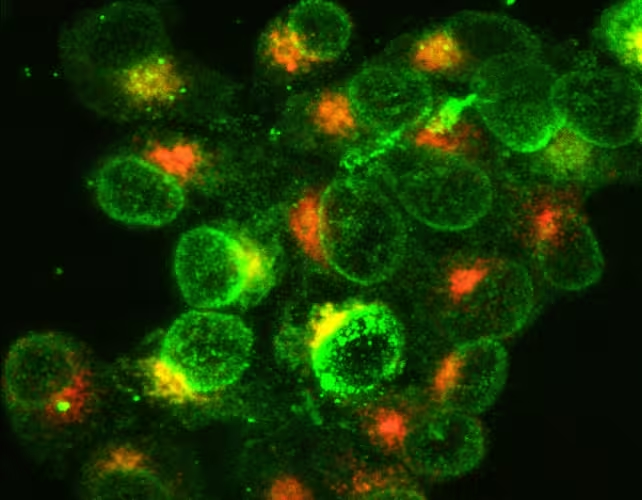
Imuninės sistemos baltieji kraujo kūneliai, aktyvuoti kovoti su bakterine infekcija. Žalia spalva rodo ant jų paviršiaus išreikštus molekulių žymenis, o oranžinė – viduje sintetinamas molekules.
Be mokslinių ir klinikinių aspektų, visuomenės sveikatos mastas yra milžiniškas: demencija paveikia daugiau nei 50 milijonų žmonių visame pasaulyje, o naujų diagnozių atsiranda kas kelias sekundes. Tai kelia didžiulį krūvį sveikatos priežiūros sistemoms, slaugos paslaugoms ir socialinei paramai. Ekonominės išlaidos, susijusios su ilgalaike priežiūra, medikamentais ir praradusiu darbingumu, reikalauja inovatyvių sprendimų, pagrįstų mechanistinėmis žiniomis apie ligos priežastis ir progresavimą.
Tyrimų prioritetai ir ateities perspektyvos
Siekiant pažangos, būtinas tarpdisciplininis požiūris, sujungiantis neurologiją, imunologiją, infekcinių ligų tyrimus, bioinorganinę chemiją ir molekulinę biologiją. Keli prioritetiniai tyrimų kryptys yra:
- Didesnės apimties longitudinalinės kohortos: Ilgalaikės studijos suteikia galimybę stebėti ankstyvus biologinius žymenis ir nustatyti priežastinius ryšius tarp imuninės aktyvacijos, infekcinių įvykių ir kognityvinių pokyčių.
- Pagerinti smegenų pralaidžius vaizdavimo agentus: PET žymenys amiloidui, tau ir mikroglijos aktyvumui, taip pat nauji MRT metodai, kurie gali matuoti uždegimą ar metabolinius pokyčius, padeda aiškinti patofiziologiją ir sekti gydymo poveikį.
- Klinikiniai tyrimai, tiesiogiai manipuliuojantys neuroimunine signala: Tai apima tiek medikamentinius bandymus, tiek imunoterapijas, kurios moduliuoja mikrogliją, komplementą ar inflammasomą. Vienu metu svarbu fiksuoti biologinius žymenis, kad būtų galima suprasti, kuriems pacientams tokia intervencija duoda naudos.
- „Omikos" analizės ir vienaląsteliniai tyrimai: Single‑cell RNA‑seq, proteomika, metabolomika ir metalomika gali išryškinti heterogeniškas ląstelių būsenas, atrasti naujus biomarkerus ir tikslus mikroglijos ar astrocitų moduliavimui.
- Tiltai tarp infekcinių ir autoimuninių mechanizmų: Reikalingi tyrimai, aiškinantys, kada Aβ veikia kaip antimikrobinis peptidas, o kada jo reakcija peržengia ribas ir virsta patologiška — tai bus esminė informacija kuriant tikslines intervencijas.
Nežymiai klaidžios, bet strateginės priemonės, tokios kaip skaitmeninės sveikatos priemonės, ankstyva diagnostika pirminėms nepakankamumo sąlygomis ir visuomenės sveikatos programos, kurios mažina infekcijos riziką (pavyzdžiui, burnos sveikatos gerinimas), taip pat gali mažinti ilgalaikę demencijos riziką.

Išvada
Žiūrint į Alzheimerio ligą per imuninę perspektyvą, išryškėja naujos prielaidos ir gydymo tikslai, kurie anksčiau buvo nuvertinti. Aβ, mikroglija, mitochondrijos, patogenai ir metalai sudaro sudėtingą tinklą, kuriame kiekvienas komponentas gali prisidėti prie ligos progresavimo arba apsaugos, priklausomai nuo laiko, genetikos ir aplinkos. Tolesni tyrimai, aiškinantys sąveikas ir biomarkerius, bei taikomosios klinikinės studijos, orientuotos į smegenų imuniteto moduliavimą, yra būtinos siekiant prevencijos ir efektyvaus gydymo šiai pasaulinei sveikatos krizei.
Šaltinis: sciencealert

Palikite komentarą