7 Minutės
Miegas ir smegenų senėjimas: apžvalga
Mes miegame maždaug trečdalį gyvenimo, tačiau miegas nėra tik pasyvus poilsio laikas. Jis palaiko fizinę atsigavimą, prisiminimų konsolidaciją ir padeda šalinti metabolinius atliekas iš smegenų. Naujausi tyrimai, pasinaudojantys aukštos raiškos magnetinio rezonanso tomografija (MRI) ir mašininio mokymosi metodais, rodo, kad lėtinis blogas miegas siejamas su smegenimis, kurios pagal vaizdinius parametrus atrodo vyresnės nei žmogaus chronologinis amžius. Toks vaizdo signalas kitose studijose buvo susijęs su didesne kognityvinio nuosmukio ir demencijos rizika.
Tyrimo dizainas ir metodika
Populiacija ir duomenų šaltiniai
Tyrėjai analizavo miego klausimynus ir smegenų MRI duomenis daugiau nei 27 000 Jungtinės Karalystės suaugusiųjų amžiaus 40–70 metų, paimtus iš didelės perspektyvinės kohortos. Toks imties dydis leido atlikti detalius statistinius modelius ir nagrinėti subtilius ryšius tarp miego modelių bei smegenų struktūros vidutinio ir ankstyvo vyresnio amžiaus grupėse. Didesnė imtis suteikė galimybę mažinti atsitiktinumo įtaką ir tikslinti niuansus tarp skirtingų socioekonominių bei sveikatos veiksnių.
Kaip apskaičiuotas smegenų amžius naudojant vaizdus ir AI
Smegenų „amžius“ buvo apskaičiuotas iš daugiau nei 1 000 atskirų vaizdinių žymių, išgautų iš struktūrinių MRI skenų. Šios žymės apėmė regioninį smegenų tūrio sumažėjimą, žievės susiaurėjimą (cortical thinning), smulkiųjų kraujagyslių pažeidimų požymius ir kitas detalizuotas morfologines savybes. Mašininio mokymosi modelis buvo išmokytas naudojant sveikiausių dalyvių skanuotes — tų, kuriems nebuvo didelių ligų — kad suformuotų tipinį vaizdinį modelį kiekvienam chronologiniam amžiui. Tada apmokytas modelis buvo pritaikytas visai kohortai, kad įvertintų kiekvieno asmens smegenų prognozuojamą amžių. Pagrindinis išmatuotas rodiklis buvo skirtumas tarp prognozuoto smegenų amžiaus ir faktinio chronologinio amžiaus (vadinamasis brain age gap). Šis skirtumas leido kiekybiškai įvertinti, ar smegenys atrodo „jaunesnės“ ar „vyresnės“ už realų amžių.
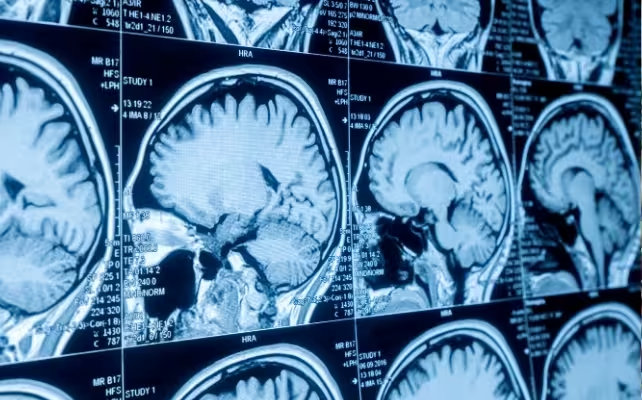
Smegenų senėjimas vertintas remiantis daugiau nei 1 000 įvairių vaizdinių žymių. (LarisaBozhikova/Getty Images/Canva)
Kaip buvo matuojamas miegas
Miegas yra daugiasluoksnis reiškinys, todėl tyrime buvo sujungta penkios savęs vertintos miego charakteristikos į sudėtinį „sveiko miego balą“:
- Chronotipas (rytinis žmogus ar vakarinis — „pelėda“)
- Tipinė miego trukmė (7–8 valandos laikomos optimaliomis)
- Nemigos simptomai
- Nuolatinis knarkimas
- Per didelis dienos mieguistumas
Dalyviai buvo suskirstyti į profilius: „sveikas“ (4–5 sveikos savybės), „tarpinis“ (2–3) ir „prastas“ (0–1). Toks multidimensinis požiūris leidžia užfiksuoti savybių tarpusavio sąveikas — pavyzdžiui, žmogus, kenčiantis nuo nemigos, dažnai taip pat nurodo dienos mieguistumą, o vakarinių tipų asmenys dažniau praneša apie trumpesnę miego trukmę.
Pagrindinės išvados
Rezultatai aiškiai siejo prastesnius miego profilius su smegenimis, kurios vaizdine išraiška atrodo vyresnės. Vidutiniškai, kiekvienam vienam sveiko miego balo taškui sumažėjus, smegenų amžiaus skirtumas padidėjo maždaug šešiais mėnesiais. Asmenys su prastu miego profiliu turėjo smegenis, kurios atrodė beveik vienu metu vyresnės nei jų chronologinis amžius, tuo tarpu turintys sveiką miego profilį rodė labai mažą arba jokį amžiaus skirtumą.
Analizuojant atskirai penkias miego charakteristikas, dvi iš jų išsiskyrė kaip stipriausi prisidėtojai prie pagreitėjusio smegenų senėjimo: vėlyvas chronotipas (įprotis dažnai gulti vėlai) ir netinkama miego trukmė (ir per trumpas, ir pernelyg ilgas miegas siejosi su blogesniais rezultatais). Tai rodo, kad tiek miego laikas, tiek jo trukmė gali būti ypač svarbūs ilgalaikei smegenų struktūrai.

Vėlyvo chronotipo asmenys — vadinamosios „pelėdos“ — gali turėti greičiau senstančias smegenis. (M_a_y_a/Getty Images Signature/Canva)
Biologiniai mechanizmai: uždegimas ir atliekų šalinimas
Yra kelios tikėtinos biologinės grandinės, paaiškinančios, kaip miego kokybė veikia smegenų senėjimą. Šios mechanikos nėra vien parduodamos hipotezės — jas palaiko eksperimentiniai ir epidemiologiniai duomenys, nors detalesnei priežasčių ir pasekmių grandinei reikia papildomų tyrimų.
- Uždegimas: Pradiniuose analizuotuose kraujo mėginiuose buvo išmatuoti cirkuliuojantys uždegiminiai žymenys. Aukštesnis uždegimas paaiškino maždaug 10 % statistinio ryšio tarp prasto miego ir vyresnės išvaizdos smegenų. Tai suderinama su hipoteze, kad miego sutrikimai didina sisteminį uždegimą, kuris savo ruožtu pažeidžia kraujagysles ir neuronus.
- Glymphatic (gliamfatinė) išsivalymo sistema: Glymphatic sistema — smegenų tinklas, atsakingas už metabolinių atliekų, tokių kaip amiloidas ir tau baltymai, šalinimą — veikia aktyviau gilaus miego metu. Sutrikęs arba nepilnavertis miegas gali trukdyti šiam procesui, skatindamas neurotoksinių baltymų kaupimąsi, kurie siejami su Alzheimerio liga ir kitomis neurodegeneracinėmis ligomis.
- Netiesioginiai kardio-metaboliniai poveikiai: Lėtinis prastas miegas didina nutukimo, 2 tipo diabeto, hipertenzijos ir kitų širdies bei kraujagyslių ligų riziką. Šios būklės yra pripažinti cerebrovaskulinio pažeidimo ir pagreitėjusio smegenų senėjimo rizikos veiksniai.
Klinikinės ir visuomenės sveikatos reikšmė
Vienerių metų skirtumas tarp matomo smegenų amžiaus ir chronologinio amžiaus gali atrodyti santykinai nedidelis, tačiau net mažas smegenų senėjimo pagreitis per dešimtmečius gali kumuliuotis ir padidinti kognityvinio pažeidimo bei demencijos tikimybę. Svarbu pažymėti, kad daugelis miego aspektų yra pakitimi. Todėl visuomenės sveikatos strategijos ir klinikinės intervencijos, gerinančios miego elgseną, gali prisidėti prie smegenų sveikatos išsaugojimo visą gyvenimą.
Praktiniai, įrodymais paremti žingsniai, kurie gali padėti, apima: nuoseklų miego tvarkaraštį, kofeino ir alkoholio ribojimą keliomis valandomis prieš miegą, vakaro ekranų laiko mažinimą ir tamsią, ramią miego aplinką. Jei įtariami nemiga, obstrukcinė miego apnėja ar kiti miego sutrikimai, reikalingas klinikinis vertinimas ir tikslinė gydymo taktika — pavyzdžiui, kognityvinė elgesio terapija nemigai ar CPAP terapija apnėjai.
Tyrimo stiprybės ir ribotumai
Tyrimo stiprybėmis laikytinas neįprastai didelis imties dydis, daugiasluoksnis miego matavimo metodas, kuris apima ne vien tik miego trukmę, ir išsamus smegenų amžiaus modelis, sukurtas iš tūkstančių MRI požymių. Tokie elementai suteikia platesnį ir jautresnį vaizdą apie tai, kaip miego elgsena gali susieti su smegenų struktūra.
Vis dėlto yra svarbių ribotumų. Tyrimas remiasi savęs pateiktais miego duomenimis, o ne objektyviais matavimais, tokiais kaip aktigrafija (actigraphy) ar polisomnografija (polysomnography), todėl gali būti klaidų, susijusių su prisiminimais ar subjektyvia percepcija. Be to, stebimosios (observacinės) dizainas negali patikimai įrodyti priežastinio ryšio. Galimi likutiniai konfundavimo veiksniai ir atvirkštinis priežastingumas — pavyzdžiui, ankstyvi smegenų pokyčiai patys gali keisti miego įpročius. Šiuos klausimus reikės spręsti ateities longitudinaliniuose tyrimuose ir intervenciniuose bandymuose.
Ekspertės įžvalga
„Šis tyrimas prideda svarbią dalį didėjančiam įrodymų krūviui, kad miegas yra esminis smegenų sveikatai,“ teigia dr. Elena Martinez, neurologė ir miego tyrėja. „Mašininio mokymosi modeliai suteikia jautrius instrumentus subtiliems struktūriniams pokyčiams aptikti. Pagrindinė išvada — miego įpročių gerinimas yra realistiška strategija lėtinti smegenų senėjimą ir gali tapti įprastos prevencinės sveikatos priežiūros dalimi kartu su mityba ir fiziniu aktyvumu.“
Ateities kryptys
Ateities tyrimų prioritetai apima objektinių miego monitoringo priemonių taikymą didelėse kohortose (pvz., aktigrafija, polisomnografija), smegenų amžiaus trajektorijų stebėjimą per ilgą laiką ir intervencinių tyrimų tyrinėjimą, ar miego sutelkta terapija (pvz., nemigos ar miego apnėjos gydymas) gali sumažinti smegenų amžiaus skirtumą ir sumažinti vėlesnę demencijos riziką. Taip pat naudingas būtų molekulinių žymenų, genetikos ir multi-omikos integravimas, kuris padėtų išaiškinti mechanizmus, susiejusius sutrikusį miegą su neurodegeneracija.
Išvados
Didelio masto tyrimas sieja prastesnį savarankiškai įvertintą miegą su smegenimis, kurios MRI ir mašininio mokymosi įvertinimuose atrodo vyresnės. Nors uždegimas tikriausiai paaiškina dalį šio ryšio, prisidėti gali keli keliai — įskaitant sutrikusią glymphatic (gliamfatinę) atliekų šalinimo sistemą ir kardio-metabolines ligas. Kadangi miegas yra pakeičiama elgsena, šie rezultatai sustiprina pranešimą, jog miegui turi būti teikiama didesnė visuomenės sveikatos reikšmė siekiant išsaugoti pažinimo funkcijas ir sklandų smegenų senėjimą. Praktinės gairės, klinikinės intervencijos ir platesnės visuomeninės programos gali padėti sumažinti smegenų sveikatos rizikas ir pagerinti ilgalaikę gyventojų gerovę.
Šaltinis: sciencealert

Palikite komentarą