7 Minutės
Įsivaizduokite miniatiūrinę širdį, kuri ne tik pati susitraukia, bet ir mažais šrifteliais atskleidžia, ką kiekviena ląstelė veikia. Tai pažadas, kurį siūlo naujausia Kanados tyrėjų sukurta širdis-ant-čipo (HOC) platforma: trimačio inžinerinio širdies audinio modelis, jungiantis bendro masto jėgos matavimus su smulkiais audinyje įterptais mikrojutikliais, kurie stebi širdies raumenų ląstelių mechaniką ir dinamiką.
Kardiologija dešimtmečius buvo ribojama svarbiausiu klausimu: neįmanoma saugiai ir be rizikos išbandyti, kaip tikra žmogaus širdis reaguos į naują vaistą ar ligą. Gyvūnų modeliai ir supaprastintos ląstelių kultūros padeda, bet praleidžia sudėtingas susitraukiančio širdies raumens mechanikas ir ląstelių heterogeniškumą. Naujas prietaisas užpildo šią spragą derindamas du papildomus matavimo sluoksnius: makro masto lankstomas kolonas, kurios lenkiasi su kiekvienu susitraukimu, ir hidrogeliu pagrįstas mikro lašelius, kurie fiksuoja lokalias įtampas tose vietose, kur ląstelės generuoja jėgas.
Kaip surenkama dvikryptė jutiklių širdis
Pradžia paprasta: imamos kamieninės ląstelės arba gyvūninės kilmės širdies ląstelės, suspenduojamos baltymų turinčiame gele ir leidžiama joms organizuotis į tankų raumeninį audinį. Tyrėjai naudojo žiurkių kardiomiocitus kartu su jungiamuoju audiniu, įtrauktus į palaikantį, ekstraląstelinę matriksą imituojantį gelį, ir užsėjo mišinį ant silicio plokštelės. Audinys savaime surenka į pulsuojantį juostą, pakabintą tarp dviejų elastingų, lankstomų kolonų. Kiekvienas susitraukimas iškreipia kolonų padėtį; nusileidimo dydis ir laikas atskleidžia viso audinio kontraktilinę galią, ritmo parametrus ir bendrą mechaninį atsaką.
Šioje stadijoje reikia kruopštaus biologinio paruošimo: ląstelių tankio optimizavimo, gelio mechaninių savybių ir kultivavimo sąlygų suderinimo, kad audinys išlaikytų ilgesnį funkcinį stabilumą. Tyrėjai atkreipė dėmesį į substrato standumą, fermentų kiekį kultūros terpėje ir elektrofiziologinį stimuliavimą, kuriuos galima reguliuoti, kad modelis imituotų tiek sveikus, tiek patologinius sutrikimus, pvz., hipertrofiją arba dilatacinę kardiomiopatiją. Tokie parametrai yra svarbūs kuriant patikimą in vitro širdies modelį, tinkamą vaistų skenavimui ir ligos mechanikos tyrimams.
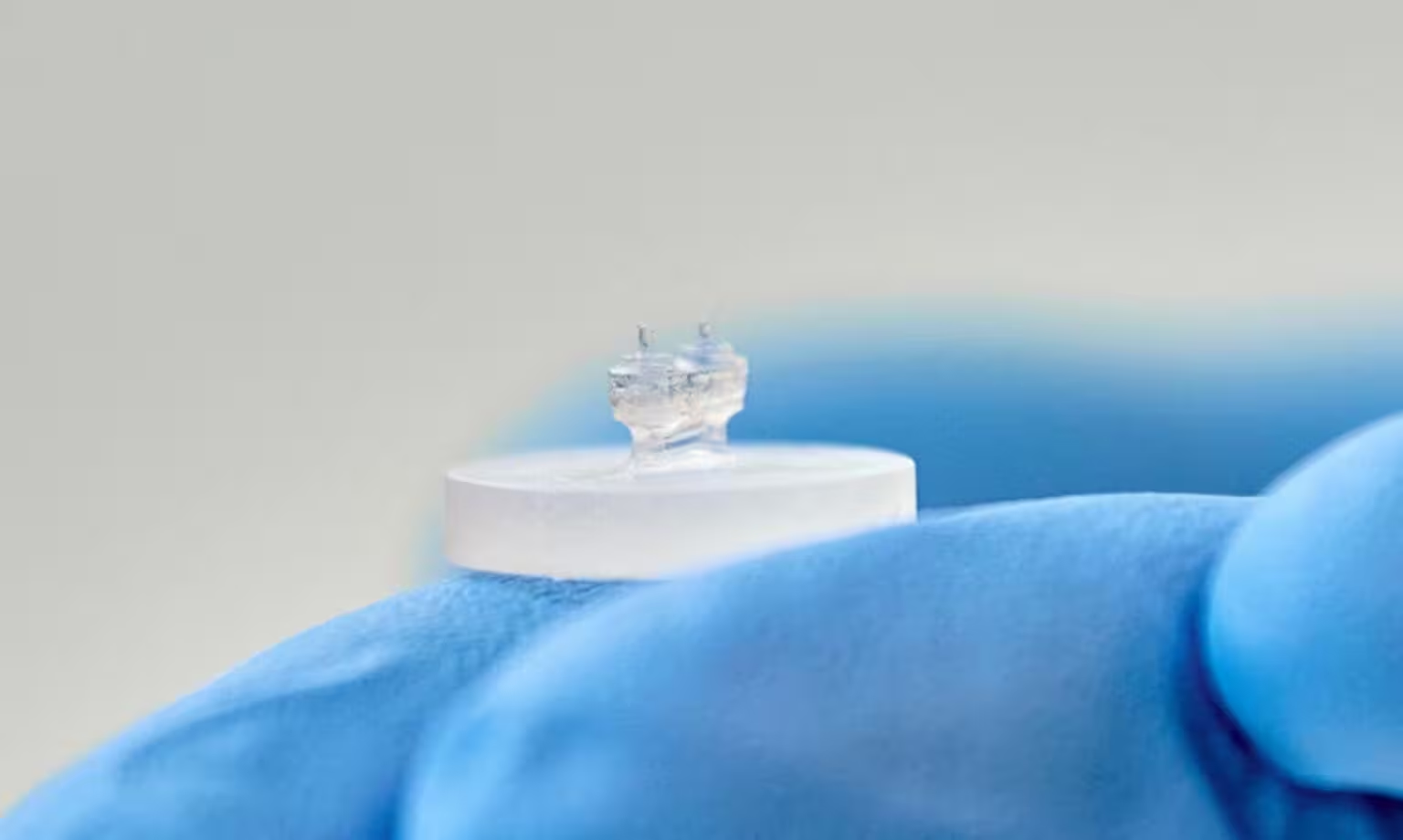
Tačiau tikroji naujovė yra mikrojutiklių sluoksnis. Smulkūs hidrogeliu užpildyti lašeliai — maždaug 50 mikrometrų skersmens — yra tolygiai paskirstyti audinio viduje. Šie mikro lašeliai deformuojasi veikiami labai mažų, lokalių jėgų, kurias generuoja pavieniai kardiomiocitai ir jų kaimyninės ląstelės. Stebėdami lašelio formos pokyčius ir judesį, komanda gali nuspėti ląstelių lygmens mechanines įtampas ir dinaminius pokyčius, kurie tradiciniuose HOC sprendimuose lieka nematomi.
Mikro lašelių chemija, hidrogelių elastingumas ir optinės savybės buvo atidžiai parinktos taip, kad lašeliai būtų pakankamai jautrūs smulkiems jėgų pokyčiams, bet kartu stabilūs ilgalaikėms stebėsenoms. Tokie lašeliai dažnai pažymimi fluorescencinėmis žymėmis arba turi skirtingą optinį kontrastą, leidžiantį juos išskirti mikroskopijoje ir automatizuotuose vaizdų analizės algoritmuose.
Jutikliai, sujungiantys skales
Kolonų sistema atsako į klausimą: kiek stipriai inžineruotas širdies raumuo susitraukia? Mikro lašeliai atsako į subtilų klausimą: kurios ląstelės prastai veikia ir kur tai vyksta? Šis skirtumas yra esminis. Daugelis širdies ir kraujagyslių ligų prasideda nuo pavienių kardiomiocitų — sutrikusio kontraktilumo, netinkamo jėgos perdavimo arba pažeistos remonto mechanikos — daug anksčiau nei sutrinka viso audinio funkcija. Dvikryptis išvestis suteikia tyrėjams ir klinikams tiek „miško“, tiek „medžių“ lygio informaciją.
Iš techninės perspektyvos toks derinys reikalauja kryžminės srities kompetencijos: inžinerijos, medžiagų mokslo, optikos, vaizdų apdorojimo ir ląstelių biologijos. Vaizdavimo duomenys iš kolonų suteikia laiko seką apie bendrą kontraktilumo jėgą ir dažnį, o mikro lašeliai duoda erdvinius ir laiko duomenis apie vietines įtempių koncentracijas ir jėgų transdukcijos pokyčius. Integruotos duomenų analizės priemonės gali sinchronizuoti abu signalus, kad būtų išskirti pvz., ar sumažėjusi kontrakcija kyla dėl pavienių ląstelių defektų, ar dėl platesnio audinio disorganizuoto jėgos perdavimo.
Farmakologija, patologijos ir precizinės strategijos
Koncepto įrodymas pasirodė, kai komanda eksponavo savo HOC platformas dviem gerai žinomiems junginiams. Norepinefrinas, adrenerginis stimuliatorius, numatomai padidino kontraktilinę jėgą ir pagreitino ritmą. Blebbistatinas, miozino inhibitorius, sumažino susitraukimus taip, kaip tikėtasi. Atsako kreivės atitiko fiziologines prognozes, todėl tai rodo, kad čipai gali tarnauti kaip patikimos preklininės platformos vaistų poveikiui kontraktilumui ir aritmogeninio pavojaus vertinimui skenuoti.
Tokie eksperimentai išryškina kelis svarbius privalumus:
- Galima tuo pačiu metu stebėti ne tik bendrą susitraukimo jėgą, bet ir lokalius mechaninius disbalansus, kurie gali būti ankstyvieji ligos požymiai.
- Modelius galima pritaikyti specifiniams kliniams scenarijams — pvz., taikyti ląsteles iš pacientų su genetinėmis aritmijomis arba dilatacine kardiomiopatija — siekiant vertinti individualų vaistų efektyvumą.
- Atsakų skirtumai tarp makro- ir mikro-skalės suteikia papildomą diagnostinę vertę, leidžiant atpažinti mechanizmus, kuriuos vienas matavimo režimas praleistų.

Kam tai naudinga? In vitro platformos, kurios tiksliai atkuria tiek audinio mechaniką, tiek ląstelių heterogeniškumą, gali pagreitinti vaistų atradimą ir padaryti testavimą saugesnį. Vietoje to, kad nepatikrintą junginį duotume pacientui, kurio širdis gali sureaguoti neprognozuojamai, klinikai galėtų anksčiau patikrinti vaisto poveikį ant paciento pačių ląstelių, išaugintų į maždaug žaislinio dydžio pulsą. Tai — personalizuota farmakologija be spėjimų.
Tyrimų grupė planuoja kitą etapą: kurti HOC modelius iš pacientų, sergančių specifinėmis širdies ligomis, tokiomis kaip dilatacinė kardiomiopatija, įgimtos ar paveldimos aritmijos ar mažai ištiriami metaboliniai raumenų sutrikimai. Tai leis modeliuoti ligos progresiją, testuoti terapijas, kurios atkurtų normalią mechaniką konkrečiam pacientui, ir identifikuoti biomarkerius, prognozuojančius gydymo reagavimą. Tokie modeliai taip pat gali būti panaudoti farmacogenomikai — nustatyti, kurie genetiniai profiliai geriausiai reaguoja į tam tikras medžiagas.
Ekspertų įžvalgos
„Stebėti ląstelių mechaniką susitraukiančiame audinyje realiu laiku iš esmės pakeičia žaidimo taisykles,“ sako Ali Mousavi, biomedicinos inžinierius ir pirmojo straipsnio autorius. „Svarbu ne tik tai, ar audinys susitraukia; svarbu, kaip ir kur jėga generuojama ir prarandama.“
Vyresnysis autorius Houman Savoji, taip pat biomedicinos inžinierius, apibrėžia platesnę viziją: „Šis dvikryptis jutiklių dizainas mus priartina prie precizinės sveikatos. Ateityje gydytojai galės pasirinkti vaistą stebėdami, kaip paciento pačių širdies audinys reaguoja ant čipo — prieš pacientui gaunant medikamentą.“
Šie prietaisai neatsisako klinikinių tyrimų ar gyvūnų modelių per naktį. Jie yra galingas papildomas įrankis: greitesnis, pigesnis ir etiškai paprastesnis nei daugelis alternatyvų, ir informatyvesnis už vienaląstelines analizės sistemas. Gebėjimas kartografuoti mechaninius veiklos sutrikimus ląstelių raiška atveria naujas kryptis suprasti randėjimą miokarde, audinių persitvarkymą esant nuolatinei įtampai ir kodėl tam tikros terapijos veikia vieniems pacientams, o kitiems — ne.
Technologijos tobulinimas apima keletą tarpusavyje susijusių sričių: medžiagų mokslo (hidrogelio formulės, ilgalaikis stabilumas), optikos (fluorescencinis ir fazinis kontrastas), inžinerijos (mikrofabrikuotos kolonėlės ir jų mechaninis kalibravimas), bei dirbtinis intelektas (vaizdų analizė ir jėgų rekonstrukcija). Kiekviena disciplina prisideda prie jautrumo, skiriamosios gebos ir plataus pritaikomumo didinimo.
Klausimai vis dar lieka: ar žmogaus kilmės audiniai pakartos tuos pačius lašelio signalus, kuriuos matė žiurkių ląstelės? Ar mikrojutiklių vaizdavimas gali būti mastelis siekiant didelio pralaidos (high-throughput) skenavimo nepadarant nuolaidų jautrumui? Ar klinikinė diagnostika ir reguliavimas gali susivienodinti su tokių platformų variacijomis tarp laboratorijų? Inžinieriai ir biologai jau iteruoja medžiagas, jutiklių chemiją ir vaizdavimo procesus, siekdami atsakyti į šiuos klausimus ir sumažinti translacijos spragą tarp laboratorijos rezultato ir klinikinės taikomosios praktikos.
Be to, etiniai ir reguliaciniai aspektai yra svarbūs: dirbtinių audinių testavimas gali sumažinti gyvūnų naudojimą, bet tuo pačiu reikalauja griežto standarto kūrimo, kad rezultatai būtų lygiaverčiai tarp centrų. Duomenų sauga ir paciento ląstelių tvarkymas taip pat turi atitikti asmens duomenų apsaugos ir biobanko praktikas.
Trumpai tariant: širdis-ant-čipo su įterptais mikro lašeliais atveria langą į gyvybės mechaniką. Ji maža, bet kalba garsiai — ir mes mokomės išgirsti. Ši platforma siūlo techninį pagrindą tiek moksliniams tyrimams apie širdies patologijas, tiek praktinius įrankius farmacijos pramonei, klinikinei diagnostikai ir personalizuotai medicinai, kai tik bus išspręstos mastelio, standarto ir reguliavimo problemos.
Šaltinis: sciencealert

Palikite komentarą